题目内容
6.芳香酯类化合物A、B互为同分异构体,均只含C、H、O三种元素.相同状况下,A、B蒸气对氢气的相对密度都是97,分子中所含氧元素的质量分数均约为0.33.已知:各有机物之间存在如下转化关系;C和D是相对分子质量相同的不同类有机物;F经连续氧化可生成C;水杨酸的结构简式为
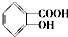 .
.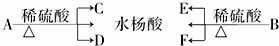
(1)A的分子式为C10H10O4.
(2)B的结构简式是
 .
.(3)完全燃烧时,1molD与1mol下列ac的耗氧量相同(填字母代号).
a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(4)C与F反应的化学方程式是HCOOH+CH3OH$→_{△}^{浓硫酸}$HCOOCH3+H2O
(5)同时符合下列要求的同分异构体有3种.
①与A互为同分异构体;
②可以水解;
③苯环上有两个取代基,且苯环上的一氯代物只有1种.
(6)1mol上述(5)中的一种有机物X,能与含4molNaOH的溶液恰好完全反应,写出此反应的化学方程式:
 .
.
分析 芳香酯类化合物A、B互为同分异构体,均只含C、H、O三种元素,A、B蒸气对氢气的相对密度是97,则二者相对分子质量为97×2=194,分子中所含氧元素的质量分数均约为0.33,则分子中O原子数为$\frac{194×0.33}{16}$=4,分子中C、H原子总相对原子质量质量为194-64=130,则$\frac{130}{12}$=10…10,故含有C、H原子数目均为10,则A、B分子式为C10H10O4.A、B水解均得到水杨酸,可知C、D碳原子总数与E、F碳原子总数相等,即均为3,F经连续氧化可生成C,说明F为醇,C为酸,C和D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,C为HCOOH,故F为CH3OH,E为CH3COOH,由此可知A为 ,B为
,B为 ,据此解答.
,据此解答.
解答 解:芳香酯类化合物A、B互为同分异构体,均只含C、H、O三种元素,A、B蒸气对氢气的相对密度是97,则二者相对分子质量为97×2=194,分子中所含氧元素的质量分数均约为0.33,则分子中O原子数为$\frac{194×0.33}{16}$=4,分子中C、H原子总相对原子质量质量为194-64=130,则$\frac{130}{12}$=10…10,故含有C、H原子数目均为10,则A、B分子式为C10H10O4.A、B水解均得到水杨酸,可知C、D碳原子总数与E、F碳原子总数相等,即均为3,F经连续氧化可生成C,说明F为醇,C为酸,C和D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,C为HCOOH,故F为CH3OH,E为CH3COOH,由此可知A为 ,B为
,B为 .
.
(1)由上述分析可知,A的分子式为C10H10O4,故答案为:C10H10O4;
(2)由上述分析可知,B的结构简式是 ,故答案为:
,故答案为: ;
;
(3)D为CH3CH2OH,改写为C2H4.H2O,而C3H6O3改写为C2H4.CO2.H2O,C3H8O改写为C3H6.H2O,C2H6O2改写为C2H2.2H2O,C3H8O、C2H6O2消耗氧气与乙醇不同,C3H6O3、C2H4 与乙醇消耗氧气相等,
故选:ac;
(4)C与F反应的化学方程式是:HCOOH+CH3OH$→_{△}^{浓硫酸}$HCOOCH3+H2O,
故答案为:HCOOH+CH3OH$→_{△}^{浓硫酸}$HCOOCH3+H2O;
(5)同时符合下列条件的同分异构体:①与A互为同分异构体;②可以水解,含有酯基;③苯环上有两个取代基,且苯环上的一氯代物只有一种,说明两个取代基相同且处于对位,符合条件的同分异构体为: 、
、 、
、 ,故答案为:3;
,故答案为:3;
(4)1mol上述(5)的同分异构体中有一种有机物X,能与含4mol NaOH溶液恰好完全反应,X为 ,此反应的化学方程式为:
,此反应的化学方程式为: ,
,
故答案为: .
.
点评 本题考查有机物的推断,关键是计算确定A、B分子式,注意根据F连续氧化生成C判断物质含有的官能团,结合分子式判断C、D含有含有碳原子数目,再结合二者相对分子质量推断,题目难度中等.

| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | 2FeO+Si$\frac{\underline{\;高温\;}}{\;}$2Fe+SiO2 | ||
| C. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
| 阳离子 | Na+ | H+ | Ba2+ |
| 阴离子 | OH- | CO32- | SO42- |
(1)C的化学式为Ba(OH)2.
(2)A溶液与B溶液反应可生成气体X,则NA个X分子的质量为44,该反应的离子方程式为2H++CO32-=H2O+CO2↑.
(3)A、B溶液分别与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为NaHSO4,鉴别B溶液中溶质电离m的阴离子的试剂为盐酸、BaCl2溶液.
②D溶于稀硝酸的离子方程式为2H++BaCO3=Ba2++H2O+CO2↑.
③D与E的混合物ag,加入足量盐酸,完全反应生成的气体在标准状况下的体积为bL,则E在混合物中的质量分数的表达式为$\frac{a-\frac{197V}{22.4}}{a}$×100%.
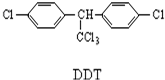
| A. | 它属于芳香烃 | B. | 分子式为C14H8Cl5 | ||
| C. | 1mol该物质能与6mol H2加成 | D. | 分子中最多可能有28个原子共面 |
| A. | HNO3 | B. | H3 PO4 | C. | H2CO3 | D. | H2 SO4 |
C2H5Cl | C2H5Br | C2H5I | |
密度(g•cm-3) | 0.897 | 1.14 | 1.25 |
沸点(℃) | 12.3 | 38.4 | 42.5 |
①沸点:50.5℃,密度:1.34g•cm-3
②沸点:10.1℃,密度:0.81g•cm-3
③沸点:21.3℃,密度:0.99g•cm-3
④沸点:7.0℃,密度:0.77g•cm-3.
| A. | ①③ | B. | ①② | C. | ②③ | D. | ②④ |