题目内容
13.硅在自然界中只以化合态形式存在,如铁矿石中的硅主要以脉石(SiO2)的形式存在,炼铁时为了除去脉石,向炼铁高炉中加入石灰石.该过程不可能涉及的化学反应是( )| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | 2FeO+Si$\frac{\underline{\;高温\;}}{\;}$2Fe+SiO2 | ||
| C. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑ | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
分析 炼铁时加入的石灰石在高温下分解生成生石灰和二氧化碳,生石灰能够与二氧化硅在反应高温条件下反应生成硅酸钙,起到造渣剂作用除去脉石;反应中生成的二氧化碳能够与碳反应生成还原剂一氧化碳,同时二氧化硅能够与焦炭发生氧化还原反应生成碳化硅和一氧化碳,据此解答.
解答 解:炼铁时加入的石灰石在高温下分解生成生石灰和二氧化碳,化学方程式:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,生成的氧化钙能够二氧化硅在反应高温条件下反应生成硅酸钙,方程式:CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3;分解生成的二氧化碳能够与碳反应生成一氧化碳,方程式:CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO,同时二氧化硅能够与焦炭发生氧化还原反应生成碳化硅和一氧化碳,方程式:SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑,因为该过程中没有单子硅,所以不能发生氧化亚铁与硅的反应,
故选:B.
点评 本题考查了高炉炼铁过程,侧重考查石灰石在高炉炼铁中作用,明确反应原理即可解答,题目难度不大.

练习册系列答案
相关题目
3.NA为阿佛加德罗常数的值,下列说法正确的是( )
| A. | 1L 0.1mol/L的氨水中有0.1NA个NH4+ | |
| B. | 在标准状况下22.4L SO3有4NA个原子 | |
| C. | 标准状况下,22.4LNO与11.2LO2混合后气体的分子数为2NA | |
| D. | 7.8g Na2S和Na2O2的混合物中所含离子数为0.3 NA |
1.下列分子中每个原子的最外层都满足8电子的是( )
| A. | F2 | B. | H2O | C. | PCl3 | D. | SO2 |
1.下表是某兴趣小组通过实验获得的稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)上述反应中,反应物的总能量比生成物的总能量高(选填“高”、“低”或“相等”).
(2)实验l、2可得出的结论是反应物浓度越大,反应速率越快;实验3、4可得出的结论是反应温度越高,反应速率越快.
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡.该金属的金属活动性比铁强(选填“强”或“弱”),铁电极上发生的电极反应式为2H++2e-=H2↑.
| 实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | V(H2SO4) mL | 溶液温度/℃ | 金属消失 的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.7 | 50 | 20 | 35 | 250 |
| 2 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
(1)上述反应中,反应物的总能量比生成物的总能量高(选填“高”、“低”或“相等”).
(2)实验l、2可得出的结论是反应物浓度越大,反应速率越快;实验3、4可得出的结论是反应温度越高,反应速率越快.
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡.该金属的金属活动性比铁强(选填“强”或“弱”),铁电极上发生的电极反应式为2H++2e-=H2↑.
5.下列有关燃料电池的说法正确的是( )
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 氢氧燃料电池工作时氢气在正极被氧化 | |
| D. | 以KOH溶液为电解质溶液的氢氧燃料电池,正极反应为O2+2H2O+4e-=4OH- |
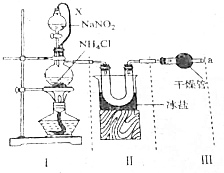 氮气、氨及铵盐用途非常广泛.回答下列问题:
氮气、氨及铵盐用途非常广泛.回答下列问题: .
.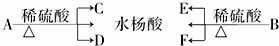
 .
. .
.