题目内容
15.某元素的气态氢化物符合通式RH3,且其水溶液呈碱性,则R的最高价氧化物的水化物的化学式是( )| A. | HNO3 | B. | H3 PO4 | C. | H2CO3 | D. | H2 SO4 |
分析 R的气态氢化物为RH3,氢化物中R元素最低负化合价为-3,则R元素最高正化合价为8-3=+5,处于VA族,结合硝酸、磷酸化学式判断.
解答 解:R的气态氢化物为RH3,氢化物中R元素最低负化合价为-3,则R元素最高正化合价为8-3=+5,处于VA族,R的最高价氧化物的水化物化学式是HRO3或H3RO4,故选AB.
点评 本题考查学生元素周期律的应用知识,难度不大,注意把握主族元素最高正价与最低负价的关系.

练习册系列答案
相关题目
5.下列有关燃料电池的说法正确的是( )
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 氢氧燃料电池工作时氢气在正极被氧化 | |
| D. | 以KOH溶液为电解质溶液的氢氧燃料电池,正极反应为O2+2H2O+4e-=4OH- |
10.下列事实与氢键有关的是( )
| A. | 水加热到很高的温度都难以分解 | |
| B. | 水结成冰体积膨胀,密度变小 | |
| C. | 水分解成氢气和氧气吸收热量 | |
| D. | HF、HCl、HBr、HI的热稳定性依次减弱 |
4.关于下列图示的说法中错误的是( )


| A. | 用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集H2气体 | |
| C. | 图③表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为放热反应 | |
| D. | 图④中的装置可形成持续稳定的电流.将锌片浸入CuSO4溶液中发生的化学反应与图④中的原电池装置反应不相同 |
5.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O
写出②中反应的化学方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl
(3)现由6种粒子Mn2+、MnO${\;}_{4}^{-}$、H+、H2O、X2Y${\;}_{8}^{2-}$(C中含有的阴离子),XY${\;}_{4}^{2-}$完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO${\;}_{4}^{-}$需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}•H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为8.4g,E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出②中反应的化学方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl
(3)现由6种粒子Mn2+、MnO${\;}_{4}^{-}$、H+、H2O、X2Y${\;}_{8}^{2-}$(C中含有的阴离子),XY${\;}_{4}^{2-}$完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO${\;}_{4}^{-}$需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}•H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为8.4g,E•xH2O的化学式为Na2C03•7H2O.
 .
.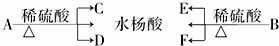
 .
. .
.