题目内容
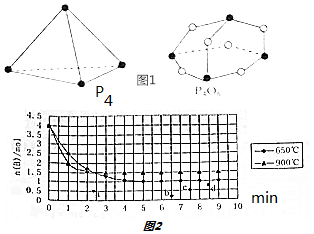
2.“关爱生命,注意安全”.惨痛的天津爆炸触目惊心,火灾之后依然火势绵延不绝的原因之一是易燃物中含有电石.工业上常用电石(主要成分为CaC2,杂质为CaS 等)与水反应生产乙炔气.(1)工业上合成CaC2主要采用氧热法.
已知:CaO(s)+3C(s)=CaC2(s)+CO(g)△H=+464.1kJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ.mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO,为维持热平衡,每生产l molCaC2,转移电子的物质的量为10.4.
(2)已知2000℃时,合成碳化钙的过程中还可能涉及到如下反应
CaO(s)+C(s)?Ca(g)+CO(g) K1△H1=a KJ•mol-1
Ca(g)+2C(s)?CaC2(s) K2△H2=b KJ•mol-1
2CaO(s)+CaC2(s)?3Ca(g)+2CO(g) K3△H3=c KJ•mol-1
则K1=$\sqrt{{K}_{2}{K}_{3}}$ (用含K2、K3的代数式表示);c=(2a-b)(用含a、b的代数式表示).
(3)利用电石产生乙炔气的过程中产生的H2S气体制取H2,既廉价又环保.
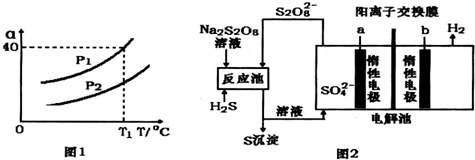
①利用硫化氢的热不稳定性制取氢气.在体积为2L的恒容密闭容器中,H2S起始物质的量为2mol,达到平衡后H2S的转化率α随温度和压强变化如图1所示.据图计算T1℃时平衡体系中H2的体积分数33.3%.由图知压强P1小于P2(填“大于”“小于”或“等于”),理由是相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2.
②电化学法制取氢气的原理如图2,请写出反应池中发生反应的离子方程式H2S+S2O82-=S↓+2SO42-+2H+,惰性电极a上发生的电极反应式为2SO42--2e-=S2O82-.
分析 (1)若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO.则为了维持热平衡,所以每生产1molCaC2,则投料的量为:1molCaO、而投入碳的量为:3mol+$\frac{464.1KJ}{110.5KJ/mol}$=7.2mol,氧气的物质的量为$\frac{464.1KJ}{110.5KJ/mol}$×$\frac{1}{2}$=2.1mol,2.1mol氧气化合价降低8.4,1molCaC2化合物价降低2.0,共降低价数为10.4mol;
(2)由反应,①CaO(s)+C(s)?Ca(g)+CO(g)△H1=a kJ•mol-1;②Ca(g)+2C(s)?CaC2(s)△H2=b kJ•mol-1;根据盖斯定律,目标反应的反应热为:①×2-②得△H3=(2a-b)kJ•mol-1,K1=$\sqrt{{K}_{2}{K}_{3}}$;
(3)①根据三步法列出起始、变化和平衡时的物质的量,再根据气体的体积分数等于气体的物质的量分数计算;相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
②反应池中H2S与S2O82-发生氧化还原反应;电解池中硫酸根离子失去电子,氢离子得到电子,以此来解答.
解答 解:(1)若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO.则为了维持热平衡,所以每生产1molCaC2,则投料的量为:1molCaO、而投入碳的量为:3mol+$\frac{464.1KJ}{110.5KJ/mol}$=7.2mol,氧气的物质的量为$\frac{464.1KJ}{110.5KJ/mol}$×$\frac{1}{2}$=2.1mol,2.1mol氧气化合价降低8.4,1molCaC2化合物价降低2.0,共降低价数为10.4mol,
故答案为:10.4;
(2)由反应,①CaO(s)+C(s)?Ca(g)+CO(g)△H1=a kJ•mol-1;②Ca(g)+2C(s)?CaC2(s)△H2=b kJ•mol-1;根据盖斯定律,目标反应=①×2-②,K1=$\sqrt{{K}_{2}{K}_{3}}$;反应热c=(2a-b)kJ•mol-1,
故答案为:$\sqrt{{K}_{2}{K}_{3}}$;(2a-b);
(3)①H2S起始浓物质的量为2mol,测定H2S的转化率,T1时H2S的转化率为40%,则
H2S(g)?H2(g)+1/2S2(g)
开始 2 0 0
转化 0.8 0.8 0.4
平衡 1.2 0.8 0.4
根据气体的体积分数等于气体的物质的量分数,P1时平衡体系中H2的体积分数=$\frac{0.8}{1.2+0.8+0.4}$×100%=33.3%;
相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
故答案为:33.3%;小于;相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
②反应池中H2S与S2O82-发生氧化还原反应,离子方程式为H2S+S2O82-=S↓+2SO42-+2H+;电解池中硫酸根离子失去电子生成S2O82-,2SO42--2e-=S2O82-,
故答案为:H2S+S2O82-=S↓+2SO42-+2H+;2SO42--2e-=S2O82-.
点评 本题考查学生化学平衡常数、盖斯定律、化学平衡移动的影响和化学方程式的书写及计算方面的知识,综合性强,题目难度中等.

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案| A. | 0.5mol/L | B. | 1mol/L | C. | 1.5mol/L | D. | 2mol/L |
| A. | Ba(OH)2═Ba2++2OH- | B. | NaHSO4═H++Na++SO42- | ||
| C. | MgCl2═Mg2++2Cl- | D. | NaHCO3═H++Na++CO32- |
| A. | BaSO4的溶解度增大,Ksp不变 | B. | BaSO4的溶解度、Ksp均增大 | ||
| C. | BaSO4的溶解度、Ksp均不变 | D. | BaSO4的溶解度不变,Ksp增大 |
 碳是形成物种最多的元素之一,许多含碳物质对人类极其重要.
碳是形成物种最多的元素之一,许多含碳物质对人类极其重要.(1)石墨烯是一种由碳原子构成的单层片状结构的新材料,结构如图所示.则12g石墨烯中含有0.5NA个6元环.
(2)工业上利用甲烷和氧气直接氧化制取甲醇的反应如下:
CH4+$\frac{1}{2}$O2(g)?CH3OH(g)△H=-128.5kJ/mol
副反应有:
CH4(g)+$\frac{3}{2}$O2(g)?CO(g)+2H2O(g)△H=a kJ/mol
CH4(g)+2O2(g)?CO2(g)+2H2O(g)△H=b kJ/mol
CH4(g)+O2(g)→HCHO(g)+H2O(g)△H=c kJ/mol
①若要有利于甲醇的生成,除了改变温度外,还可以采取的两种措施是增大压强、选用合适的催化剂;
②甲醇与氧气反应生成HCHO(g)和水蒸汽的热化学方程式为CH3OH(g)+1/2O2(g)→HCHO(g)+H2O(g)△H=(c+128.5)KJ•L-1.
(3)苯乙烷(C8H10)生产苯乙烯(C8H8)的反应:C8H10(g)?C8H8(g)+H2(g)△H>0.T1℃下,将0.40mol苯乙烷充入2L密闭容器中反应,不同时间容器内n(C8H10)如下表:
| 时间/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
②改变温度为T2℃,其他条件不变,测得平衡时容器内气体压强为反应前的1.4倍,则此时苯乙烷的转化率为40%.
(4)用惰性电极电解葡萄糖和硫酸钠混合溶,可以制得葡萄糖酸[CH2OH(CHOH)4COOH]和己六醇[CH2OH(CHOH)4CH2OH].葡萄糖酸在阳极生成,对应的电极反应式CH2OH(CHOH)4CHO+H2O-2e-═CH2OH(CHOH)4COOH+2H+.
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
| A. | 0~5min 时用H2O(g)表示的平均反应速率为1.2×10-3 mol/( L.min) | |
| B. | 5min~10min 改变的条件是再加入了0.1mol H2O(g) | |
| C. | 200℃时,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.01molCO2(g)、0.01molH2(g),达平衡时,CO(g)为1.2×10-3mol/L | |
| D. | 300℃时,若向容器中充入0.01mol CO(g)、0.01mol H2O(g)、0.02molCO2(g)、0.02molH2(g),则开始反应时ν(正)<ν(逆) |
(1)已知CO和H2的燃烧热分别是283.0kJ/mol、285.8kJ/mol,lg液态水变成水蒸气时要吸收2.44kJ的热量;则该反应的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.12kJ/mol;.
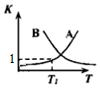
(2)该反应随温度升高正、逆反应平衡常数的变化曲线如图所示,表示K正的曲线为B(选填“A”或“B”),理由是正反应为放热反应,升高温度,平衡向逆向移动,K值减小.
(3)T1℃时,向容积固定为5L的容器中充入2mol水蒸气和3molCO,发生上述反应达平衡,则平衡时水蒸气的转化率是60%(填字母)
(4)保持温度为T1℃,改变水蒸气和CO的初始物质的量之比,充入恒容容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填字母)
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a molH2
d.混合气中 n(CO):n(H2O):n(CO2):n(H2)=9:4:6:6
(5)某工业合成氨的原料气组成为:H240%、N220%、CO30%、CO210% (均为体积分数).向上述原料气中加入水蒸气,以除去其中的CO.己知不同温度下的反应物投料比[$\frac{n({H}_{2}0)}{n(C0)}$],平衡时混合气体中CO的体积分数如表所示:
| CO体积分数% 投料比 | 温度/℃ | ||||
| 200 | T2 | T3 | T4 | ||
| $\frac{n({H}_{2}0)}{n(C0)}$ | 1 | 1.70 | 2.73 | 6.00 | 7.85 |
| 3 | 0.21 | 0.30 | 0.84 | 1.52 | |
| 5 | 0.02 | 0.06 | 0.43 | 0.80 | |
②维持温度不变,若要使CO的转化率升高,可以改变的条件是加水/增大H2O和CO投料比/减小生成物浓度(分离出产物).
③温度为T3℃、$\frac{n({H}_{2}0)}{n(C0)}$=1时,变换后的平衡混合气体中H2的体积分数是47.8%.
| A. | 无色溶液:Al3+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、NH4+、Fe3+、NO3- | |
| C. | FeCl3溶液:K+、Na+、NO3-、SCN- | |
| D. | 由水电离出的C(H+)=10-13mol/L的溶液:Na+、K+、SiO32-、NO3- |