题目内容
7.已知P4(白磷)+3O2=P4O6.△H=-1632kJ/mol;白磷和P4O6的分子结构如图1所示,其中部分键能数据如下:P-O:360kJ/mol,O=O:498kJ/mol,则断开1molP-P所吸收的热量为199kJ.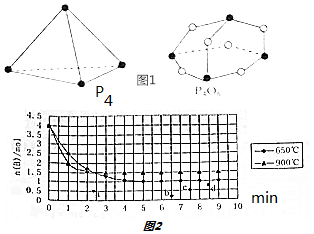
(2)Mg存在于叶绿素中,某些作物生长需要输镁肥,从海水中提取镁是获得镁的主要来源.常温下,已知Mg(OH)2的Ksp=1.6×10-11,某浓缩海水中MgCl2浓度为1.6×10-3mol/L,则要使Mg2+形成Mg(OH)2沉淀,则溶液的pH至少要达到10.
(3)将A(g)和B(g)按照物质的量比为1:1通入到体积为2L的恒容密闭容器中,进行反应A(g)+B(g)?M(g)+N(g),数据变化如图2所示:
①上述反应为放热(填“吸热”或“放热”)反应;
②计算在650℃下,从开始到平衡的反应速率v(A)=0.375mol/(L.min);
③在900℃下该反应的平衡常数为2.78(保留三位有效数字),若平衡后保持温度不变向容器中继续充入2molA、1molM和1molN,这时平衡正向移动.(填“正向”、“逆向”“不”);
④若650℃时在同样容器中起始时充入的A和B的物质的量均为2mol,则图2中c是B物质平衡时对应的点.
分析 (1)焓变等于反应物总键能-生成物总键能,据此计算P-P键的键能;
(2)镁离子沉淀时c(OH-)=$\sqrt{\frac{{K}_{sp}[Mg(OH)_{2}]}{c(M{g}^{2+})}}$=$\sqrt{\frac{1.6×1{0}^{-11}}{1.6×1{0}^{-3}}}$mol/L=10-4 mol/L,c(H+)=$\frac{1{0}^{-14}}{1{0}^{-4}}$mol/L=10-10 mol/L,pH=-lgc(H+);
(3)①升高温度平衡向吸热方向移动;
②反应达到平衡状态时△n(B)=(4-1)mol=3mol,根据方程式知,参加反应的△n(A)=△n(B)=3mol,从开始到平衡的反应速率v(A)=$\frac{\frac{△n}{V}}{△t}$;
③反应达到平衡状态时c(A)=$\frac{1.5mol}{2L}$=0.75mol/L,开始时c(A)=c(B)=$\frac{4mol}{2L}$=2mol/L,
该反应中A(g)+B(g)?M(g)+N(g)
开始(mol/L)2 2 0 0
反应(mol/L)1.25 1.25 1.25 1.25
平衡(mol/L)0.750.75 1.25 1.25
化学平衡常数K=$\frac{c(M).c(N)}{c(A).c(B)}$;
根据浓度商与化学平衡常数相对大小确定反应方向;
④若650℃时在同样容器中起始时充入的A和B的物质的量均为2mol,相当于减小压强平衡不移动,其转化率相等,但反应速率减小,反应达到平衡时间延长,达到平衡浓度是原来一半.
解答 解:(1)焓变等于反应物总键能-生成物总键能,设P-P键的键能为xkJ/mol,
6x+3×498-12×360=-1632,x=199,断键吸收热量,
故答案为:吸收;199;
(2)镁离子沉淀时c(OH-)=$\sqrt{\frac{{K}_{sp}[Mg(OH)_{2}]}{c(M{g}^{2+})}}$=$\sqrt{\frac{1.6×1{0}^{-11}}{1.6×1{0}^{-3}}}$mol/L=10-4 mol/L,c(H+)=$\frac{1{0}^{-14}}{1{0}^{-4}}$mol/L=10-10 mol/L,pH=-lgc(H+)=-lg10-10=10,
故答案为:10;
(3)①升高温度平衡向吸热方向移动,根据图知,升高温度B的物质的量增大,说明平衡逆向移动,则正反应是放热反应,故答案为:放热;
②反应达到平衡状态时△n(B)=(4-1)mol=3mol,根据方程式知,参加反应的△n(A)=△n(B)=3mol,从开始到平衡的反应速率v(A)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{3mol}{2L}}{4min}$=0.375mol/(L.min),
故答案为:0.375mol/(L.min);
③反应达到平衡状态时c(A)=$\frac{1.5mol}{2L}$=0.75mol/L,开始时c(A)=c(B)=$\frac{4mol}{2L}$=2mol/L,
该反应中A(g)+B(g)?M(g)+N(g)
开始(mol/L)2 2 0 0
反应(mol/L)1.25 1.25 1.25 1.25
平衡(mol/L)0.750.75 1.25 1.25
化学平衡常数K=$\frac{c(M).c(N)}{c(A).c(B)}$=$\frac{1.25×1.25}{0.75×0.75}$=2.78;
继续充入2molA、1molM和1molN,c(A)=0.75mol/L+$\frac{2mol}{2L}$=1.75mol/L、c(M)=c(N)=1.25mol/L+$\frac{1mol}{2L}$=1.75mol/L,
浓度商=$\frac{1.75×1.75}{1.75×0.75}$=2.3<2.78,平衡正向移动,
故答案为:2.78;正向;
④若650℃时在同样容器中起始时充入的A和B的物质的量均为2mol,相当于减小压强平衡不移动,其转化率相等,但反应速率减小,反应达到平衡时间延长,达到平衡浓度是原来一半,则c点是B物质平衡时对应的点,故答案为:c.
点评 本题考查化学平衡计算、难溶物溶解平衡等知识点,侧重考查学生图象分析、计算及综合知识灵活运用能力,会根据浓度商与化学平衡常数相对大小确定反应方向,注意(3)③可以等效为减小压强,注意白磷分子中含有6个P-P键而不是4个P-P键,为易错点,题目难度中等.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案| A. | ①③ | B. | ②④ | C. | ①④ | D. | ①②③ |
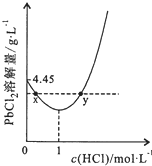 20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g•L-1)如图所示.下列叙述正确的是( )
20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g•L-1)如图所示.下列叙述正确的是( )| A. | 盐酸浓度越大,Ksp(PbCl2)越大 | |
| B. | PbCl2能与一定浓度的盐酸反应 | |
| C. | x、y两点对应的溶液中c(Pb2+)相等 | |
| D. | 往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s) |
(1)煤制天然气时会发生多个反应,生产过程中有多种途径生成CH4.
已知:C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
CO(g)+3H2(g)?CH4(g)+H2O(g)△H=-203kJ•mol-1
写出CO与H2O(g)反应生成H2和CO2的热化学方程式CO(g)+H2O(g)=H2(g)+CO2(g),△H=-41kJ/mol.
(2)天然气中含有H2S杂质,某科研小组用氨水吸收得到NH4HS溶液,
已知T℃,k(NH3•H2O)=1.74×10-5,k1(H2S)=1.07×10-7,k2(H2S)=1.74×10-13,NH4HS溶液中所含粒子浓度大小关系正确的是ac.
a.[NH4+]>[HS-]>[OH-]>[H+]b.[HS-]>[NH4+]>[S2-]>[H+]
c.[NH4+]>[HS-]>[H2S]>[H+]d.[HS-]>[S2-]>[H+]>[OH-]
(3)工业上常用CH4与水蒸气在一定条件下来制取H2,其原理为:CH4(g)+H2O(g)═CO(g)+3H2(g).
①该反应的逆反应速率表达式为:v=kc(CO)c3(H2),k为速率常数,在某温度下,测得实验数据如表:
| CO浓度(mol•L-1) | H2浓度(mol•L-1) | 逆反应速率(mol•L-1•min-1) |
| 0.1 | c1 | 9.6 |
| c2 | c1 | 19.2 |
| c2 | 0.3 | 64.8 |
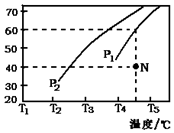
②在体积为2L的密闭容器中通入物质的量均为2mol的CH4和水蒸气,在一定条件下发生反应,测得H2的体积分数与温度及压强的关系如图2所示,则压强P1大于P2(填“大于”或“小于”);温度T3小于T4(填“大于”或“小于”);
③压强为P1时,在N点:v正大于v逆(填“大于”、“小于”或“等于”). 求N点对应温度下该反应的平衡常数K=48.
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ•mol-1) | 436 | 945 | 391 |
②若将1mol N2和3mol H2放入一密闭容器中在催化剂存在下进行反应,理论上放出或吸收的热量为Q1,而在实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是A.
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2.
| A. | MnO2 | B. | Fe3O4 | C. | MgO | D. | Cr2O3 |
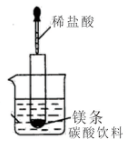 (1)如图所示(夹持仪器省去),把试管放入盛有20℃碳酸饮料的烧杯中,试管中开始放入几块镁条,再用滴管滴加5ml的盐酸于试管中.
(1)如图所示(夹持仪器省去),把试管放入盛有20℃碳酸饮料的烧杯中,试管中开始放入几块镁条,再用滴管滴加5ml的盐酸于试管中.