��Ŀ����
2��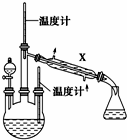 ������Ҫ�Ļ���ԭ�ϣ�ij̽��С���������з�Ӧ��ȡˮ���£�N2H4•H2O����CO��NH2��2+2NaOH+NaClO�TNa2CO3+N2H4•H2O+NaCl
������Ҫ�Ļ���ԭ�ϣ�ij̽��С���������з�Ӧ��ȡˮ���£�N2H4•H2O����CO��NH2��2+2NaOH+NaClO�TNa2CO3+N2H4•H2O+NaClʵ��һ���Ʊ�NaClO��Һ
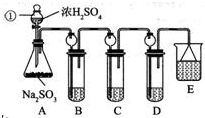
��1��������ͨ�뵽ʢ��NaOH��Һ����ƿ�У���ƿ�з�����Ӧ�����ӷ���ʽΪCl2+2OH-=ClO-+Cl-+H2O��
ʵ�������ȡˮ���£�ʵ��װ����ͼ��ʾ��
���Ʒ�Ӧ�¶ȣ�����Һ©���е���Һ��������������ƿ�У���ַ�Ӧ����������������ƿ�ڵ���Һ���ռ�108��114����֣�����֪��N2H4•H2O+2NaClO�TN2��+3H2O+2NaCl��
��2������X�������ǣ�ֱ�Σ������ܣ���Һ©���е���Һ��A���A����B������
A��NaOH��NaClO�����Һ
B��CO��NH2��2��Һ
ѡ����������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ��������������
ʵ�������ⶨ�����ˮ���µ���������
ˮ���¾��л�ԭ�ԣ����������ɵ������ⶨˮ���µ����������ɲ������в��裺
a����ȡ���5.000g����������NaHCO3���壬��ϡ�͡�ת�ơ����ݵȲ��裬����250mL��Һ��
b����ȡ25.00mL��Һ����ƿ�У�����10mLˮ��ҡ�ȣ�
c����0.2000mol•L-1����Һ�ζ�����Һ������ɫ�Ұ�����ڲ���ʧ���ζ������У���Һ��pH������6.5���ң���¼���ĵ�ı���Һ�������
d����һ�����������ݴ�����
��3��ˮ���������Һ��Ӧ�Ļ�ѧ����ʽΪN2H4•H2O+2I2=N2��+4HI+H2O���ⶨ�����У�NaHCO3�ܿ�����Һ��pH��6.5���ң�ԭ�������ɵ�HI��NaHCO3 ��Ӧ��
��4���ζ�ʱ����ı���Һʢ������ʽ�����ʽ����ʽ�����ζ����У������εζ����ĵ�ı���Һ��ƽ�����Ϊ18.00mL���������ˮ���£�N2H4•H2O������������Ϊ18.0%��������λ��Ч���֣���
���� ��1������ͨ�뵽ʢ��NaOH����ƿ�з�����Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��2������װ��ͼ��֪����X�����ƣ�������ȡˮ���£�N2H4•H2O���ķ�Ӧԭ��Ϊ��CO��NH2��+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl����Ϸ�Ӧ����ͷ�Ӧ������жϣ�ˮ���£�N2H4•H2O�����л�ԭ�ԣ��ױ���������������
��3��ˮ���������Һ��Ӧ����������ԭ��Ӧ�����ɵ������⻯���ˮ��NaHCO3�ܿ�����Һ��pH��6.5���ң�����Ϊ̼�����ƺ͵⻯�ⷴӦ��
��4���ⵥ�ʾ��������ԣ�ѡ����ʽ�ζ���ʢװ����ʵ�飻��Ϸ�Ӧ������ϵ����õ������ˮ���£�N2H4•H2O��������������
��� �⣺��1������ͨ�뵽ʢ��NaOH����ƿ�з�����Ӧ�����Ȼ��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪ��Cl2+2OH-=ClO-+Cl-+H2O��
�ʴ�Ϊ��Cl2+2OH-=ClO-+Cl-+H2O��
��2������װ��ͼ��֪����X������Ϊ ��ֱ�Σ������ܣ�������ȡˮ���£�N2H4•H2O���ķ�Ӧԭ��Ϊ��CO��NH2��+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl����Ϸ�Ӧ����ͷ�Ӧ������жϣ���Һ©���е���Һ��NaOH��NaClO�����Һ��ˮ���£�N2H4•H2O�����л�ԭ�ԣ��ױ����������������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ��������������
�ʴ�Ϊ����ֱ�Σ������ܣ�A���������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ��������������
��3��ˮ���������Һ��Ӧ����������ԭ��Ӧ�����ɵ������⻯���ˮ����Ӧ�Ļ�ѧ����ʽΪ��N2H4•H2O+2I2=N2��+4HI+H2O��NaHCO3�ܿ�����Һ��pH��6.5���ң�����Ϊ̼�����ƺ͵⻯�ⷴӦ��
�ʴ�Ϊ��N2H4•H2O+2I2=N2��+4HI+H2O�����ɵ�HI��NaHCO3 ��Ӧ��
��4���ⵥ�ʾ��������ԣ�ѡ����ʽ�ζ���ʢװ����ʵ�飻��Ϸ�Ӧ������ϵ����õ������ˮ���£�N2H4•H2O��������������
N2H4•H2O+2I2=N2��+4HI+H2O��
1 2
n 0.2000mol/L��0.018L
n=0.0018mol
250ml��Һ�к��е����ʵ���=0.0018mol��$\frac{250}{25}$=0.018mol
ˮ���£�N2H4•H2O������������=$\frac{0.018mol��50g/mol}{5.00g}$��100%=18.0%
�ʴ�Ϊ����ʽ��18.0%��
���� ���⿼���������Ʊ������ʵ�ʵ���������֤����Ӧ�ã���Ҫ�ǹ��̷����жϣ����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


| A�� | K�պ�ʱ��c�缫��Ӧʽ��PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B�� | ����·��ת��0.4mol����ʱ��I�����ĵ�H2SO4Ϊ0.2 mol | |
| C�� | K�պ�ʱ��II��SO42-��c�缫Ǩ�� | |
| D�� | K�պ�һ��ʱ���II�ɵ�����Ϊ��Դ��d�缫Ϊ���� |
| A�� | 0.1 mol•L-1��BaCl2��Һ�У�K+��Na+��OH-��NO3- | |
| B�� | ʹ���ȱ�����Һ�У�Ca2+��NH4+��CH3COO-��Cl- | |
| C�� | ��ɫ������Һ�У�Fe2+��SO42-��NO3-��Na+ | |
| D�� | ��ˮ�������c��H+��=10-12 mol•L-1����Һ�У�Mg2+��K+��Br-��HCO3- |
| A�� | [H+]��С����Һһ���ʼ��� | |
| B�� | pH=7����Һһ�������� | |
| C�� | [OH-]=[H+]����Һһ�������� | |
| D�� | ����ʹ��̪��Һ������Һһ�������� |
| A�� | ��Կ��ȡ�������������̷�ĩ | |
| B�� | ��ȼ�ŵľƾ�����ֱ�����Ӿƾ� | |
| C�� | ʵ���Ҽ��ȸ��������������װ����ȡ���� | |
| D�� | ʵ���ҽ����������Ʊ�����ú���� |
| A�� | ���³�ѹ�£�11.2 L�������е�ԭ����ĿΪNA | |
| B�� | п���������û���1 mol H2��ת�Ƶĵ�����ĿΪNA | |
| C�� | 4.4 g ������̼���еķ�����ĿΪ0.1 NA | |
| D�� | 1 mol/L CaCl2��Һ�к��е���������ĿΪ2NA |
| A�� | NH4HCO3��Һ�м�������NaOH��Һ���ȣ�NH+4+OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O | |
| B�� | ����������Ũ���ᷴӦ��Fe+6H++3NO3-�TFe3++3NO2��+3H2O | |
| C�� | ��������������Һ�м���������⣺2Fe2++H2O2+2H+�T2Fe3++2H2O | |
| D�� | ��ʳ���ܽ�ˮ����CaCO3+2H+�TCa2++CO2��+H2O Mg��OH��2+2H+�TMg2++2H2O |