题目内容
19.在一密闭容器中,反应 mA(g)?nB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | 物质B的质量分数减小了 | D. | m 小于n |
分析 先假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的60%,比假设大,说明平衡向生成B的方向移动,即减小压强平衡向正反应方向移动,则m<n,据此结合选项判断.
解答 解:A.先假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的60%,比假设大,说明平衡向生成B的方向移动,即平衡向正反应方向移动,故A错误;
B.根据A的判断,平衡向生成B的方向移动,即减小压强平衡向正反应方向移动,反应物转化率增大,故B错误;
C.平衡向正反应移动,B的质量增大,混合气体的总质量不变,故物质B的质量分数增大,故C错误;
D.减小压强平衡向体积增大的方向移动,根据A的判断,平衡向生成B的方向移动,减小压强平衡向正反应方向移动,则m<n,故D正确;
故选D.
点评 本题考查化学平衡移动知识,题目难度不大,注意利用假设法分析、判断平衡移动方向.

练习册系列答案
相关题目
10.在密闭容器中发生反应:aX(气)+bY(气)?cZ(气)+dW(气),反应达到平衡后,保持温度不变,将气体压缩到原来的$\frac{1}{2}$体积,当再次达到平衡时,W的浓度为原平衡的1.8倍,下列叙述中正确的是( )
| A. | 平衡常数K增大 | B. | a+b<c+d | C. | X的转化率下降 | D. | Z的体积分数增加 |
14.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 达到化学平衡时,4 v正(O2)=5 v逆(NO) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 达到平衡时,若减小容器体积,则NH3的转化率会增大 |
4.下列变化属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 活性炭吸附冰箱中的异味 | ||
| C. | 分离液态空气制氧气 | D. | 海水晒盐 |
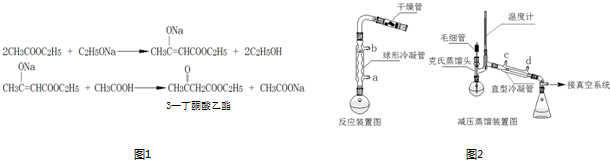
 CH3COOCH2CH3+H2O,反应类型是酯化反应.
CH3COOCH2CH3+H2O,反应类型是酯化反应.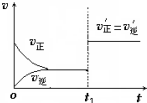 在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).
在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).