题目内容
13.用0.005mol/LHCl溶液中和50mLpOH=3的下列碱溶液,消化HCl溶液体积最大的是( )| A. | 氨水 | B. | 氢氧化钠 | C. | 氢氧化钡 | D. | 氢氧化钙 |
分析 pOH=3的碱溶液中,c(OH-)=0.001mol/L,则50mL的任意pOH=3的碱溶液中n(OH-)=0.001mol/L×0.05L=5×10-5mol.而一水合氨为弱电解质,不能完全电离,而氢氧化钠、氢氧化钡和氢氧化钙均为强电解质,完全电离,故四种碱溶液的氢氧根的总量不同,据此分析.
解答 解:pOH=3的碱溶液中,c(OH-)=0.001mol/L,则50mL的任意pOH=3的碱溶液中电离出的n(OH-)=0.001mol/L×0.05L=5×10-5mol.
而一水合氨为弱电解质,不能完全电离,故氨水的总物质的量大于5×10-5mol;而氢氧化钠、氢氧化钡和氢氧化钙均为强电解质,完全电离,即这三种碱溶液中的氢氧根均为5×10-5mol,故四种碱溶液中消耗盐酸体积最大的是氨水.
故选A.
点评 本题依托酸碱中和反应的有关计算考查了弱电解质的电离平衡,难度不大,应注意的是当pOH相同时,溶液浓度不一定相同.

练习册系列答案
相关题目
3.化学已渗透到人类生产生活的各个方面,下列说法合理的是( )
| A. | PM2.5含有的铅、铬、镉、钒、砷等对人体有害的元素均是金属元素 | |
| B. | 绿色化学的核心是利用化学原理减少和消除工业生产对环境的污染 | |
| C. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| D. | 二氧化硫的大量排放是造成光化学烟雾的主要原因 |
4.已知 25℃时有关弱酸的电离平衡常数如下:
常温下,下列各溶液的叙述中正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数( 25℃) | Ka=1.8×10-5 | Ka=4.9×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| A. | pH=a 的 CH3COOH 溶液,稀释 10 倍后,其 pH=b,则 a+1<b | |
| B. | pH=5 的 H2CO3 溶液中,c(H+)=c(HCO3-)=1×10-5 mol/L | |
| C. | pH相同的①CH3COONa ②NaHCO3 ③NaCN 三种溶液的 c(Na+):①>②>③ | |
| D. | 等浓度等体积的①CH3COONa 和②NaCN 溶液,溶液中阴离子数目:②>① |
8.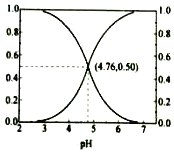 25℃时,在含CH3COOH和CH3COOˉ的溶液中,CH3COOH和CH3COOˉ二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示.下列说法不正确的是( )
25℃时,在含CH3COOH和CH3COOˉ的溶液中,CH3COOH和CH3COOˉ二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示.下列说法不正确的是( )
 25℃时,在含CH3COOH和CH3COOˉ的溶液中,CH3COOH和CH3COOˉ二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示.下列说法不正确的是( )
25℃时,在含CH3COOH和CH3COOˉ的溶液中,CH3COOH和CH3COOˉ二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示.下列说法不正确的是( )| A. | 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH) | |
| B. | 在pH=7的溶液中,α(CH3COOH)=0,α(CH3COO-)=1.0 | |
| C. | 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+) | |
| D. | 在pH=4.76的溶液中加盐酸,α(CH3COOH)与α(CH3COO-)之和保持不变 |
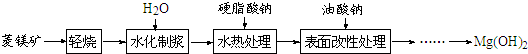
1.由菱镁矿(主要成分为MgCO3)制阻燃型氢氧化镁的工艺流程如下:
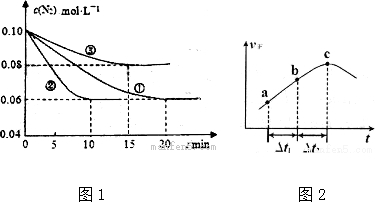
(1)从图1和图2可以得出的结论为随着水化时间延长,MgO的量不断减少,Mg(OH)2的量不断增加、温度升高,水化反应速率加快.

(2)水化反应MgO+H2O═Mg(OH)2能自发进行的原因是△H<0.
(3)结合元素周期律和下表可知,金属氢氧化物受热分解的规律有金属离子半径越大,氢氧化物越难分解(或金属性越强,氢氧化物越难分解等).(写一条即可)
部分主族元素的金属氢氧化物热分解温度/℃
(4)已知热化学方程式:Mg(OH)2(s)═MgO(s)+H2O(g)△H=+81.5kJ•mol-1
①Mg(OH)2起阻燃作用的主要原因是Mg(OH)2分解时吸热,使环境温度下降;同时生成的耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳.
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是无烟、无毒、腐蚀性小.

(1)从图1和图2可以得出的结论为随着水化时间延长,MgO的量不断减少,Mg(OH)2的量不断增加、温度升高,水化反应速率加快.

(2)水化反应MgO+H2O═Mg(OH)2能自发进行的原因是△H<0.
(3)结合元素周期律和下表可知,金属氢氧化物受热分解的规律有金属离子半径越大,氢氧化物越难分解(或金属性越强,氢氧化物越难分解等).(写一条即可)
部分主族元素的金属氢氧化物热分解温度/℃
| LiOH | NaOH | KOH | Al(OH)3 | Mg(OH)2 | Ca(OH)2 | Ba(OH)2 |
| 924 | 不分解 | 不分解 | 140 | 258 | 390 | 700 |
①Mg(OH)2起阻燃作用的主要原因是Mg(OH)2分解时吸热,使环境温度下降;同时生成的耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳.
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是无烟、无毒、腐蚀性小.
5.下列关于卤素的说法正确的是( )
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 氧化性Cl2>Br2>I2还原性Cl->Br->I- | |
| C. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| D. | 氯水具有酸性,能使紫色石蕊试剂先变红后褪色,也可用pH试纸测量其pH值 |
 .
.
 实验室用氢氧化钠固体配制1.0mol•L-1的NaOH溶液250mL,回答下列问题:
实验室用氢氧化钠固体配制1.0mol•L-1的NaOH溶液250mL,回答下列问题: