题目内容
1.A、B、C、D、E 是核电荷数依次增大的五种短周期主族元素,A 元素的原子核内只 有 1 个质子;B 元素的原子半径是其所在主族中最小的,B 的最高价氧化物对应水化物的化学式为 HBO3;C 元素原子的最外层电子数比次外层多 4;C 的阴离子与 D 的阳离子具有相同的电子排布,两元素可形成化合物 D2C;C、E 同主族.(1)B 在周期表中的位置为第二周期第VA族.
(2)E 元素形成的氧化物对应的水化物的化学式为H2SO3、H2SO4.
(3)元素 B、C、D、E 形成的简单离子半径大小关系是S2->N3->O2->Na+(用离子符号表 示).
(4)用电子式表示化合物 D2C 的形成过程:
 .
.(5)由 A、B、C 三种元素形成的离子化合物的化学式为NH4NO3,它与强碱溶液共热,发生反应的离子方程式是NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(6)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此 反应的化学方程式为4Na2SO3=Na2S+3Na2SO4(化学式用具体的元素符号表示).
(7)E 的某种氧化物是大气污染物之一,也是某工业生产中的主要尾气之一.某校兴趣 小组欲采用下列方案测定此工业尾气中的 E 的氧化物的含量
尾气(VL)$→_{①}^{过量H_{2}O_{2}溶液}$溶液$→_{②}^{过量Ba(OH)_{2}溶液}$$→_{③}^{过滤、洗涤、干燥、称量}$固体(mg)
通过的尾气体积为 VL(已换算成标准状况)时,该尾气中 E 的氧化物含量(体积分数)为$\frac{22.4m}{233v}$(用含有 V、m 的代数式表示).
分析 A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,则A为H元素;B元素的原子半径是其所在主族中最小的,处于第二周期,B的最高价氧化物对应水化物的化学式为HBO3,B元素最高正价为+5,故B为N元素;C元素原子的最外层电子数比次外层多4个,原子只能有2个电子层,最外层电子数为6,故C为O元素;C的阴离子与D的阳离子具有相同的电子排布,离子核外电子数为10,两元素可形成化合物D2C,D元素化合价为+1,处于IA族,故D为Na;C、E同主族,则E为S元素,据此解答.
(1)由原子结构示意图,确定元素在周期表中的位置,最外层电子数即主族序数,电子层数即周期序数;
(2)E为S元素,对应的氧化物的水化物有H2SO3、H2SO4;
(3)据电子层数越多,半径越大,具有相同的核外电子排布的核大径小分析;
(4)据D2C为Na2O,为离子化合物,故电子式表示的形成过程为 ;
;
(5)据A、B、C为H、N、O形成的盐为NH4NO3,加热条件下,与强碱溶液反应生成氨气来书写离子方程式;
(6)据D2EC3形成的盐应为Na2SO3并根据题意确定方程式;
(7)通过硫酸钡的量,并根据S元素守恒得到硫的氧化物的量.
解答 解:A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,则A为H元素;B元素的原子半径是其所在主族中最小的,处于第二周期,B的最高价氧化物对应水化物的化学式为HBO3,B元素最高正价为+5,故B为N元素;C元素原子的最外层电子数比次外层多4个,原子只能有2个电子层,最外层电子数为6,故C为O元素;C的阴离子与D的阳离子具有相同的电子排布,离子核外电子数为10,两元素可形成化合物D2C,D元素化合价为+1,处于IA族,故D为Na;C、E同主族,则E为S元素.
(1)B为N元素,原子核外有2个电子层,最外层电子数为5,则位于周期表中第二周期ⅤA族;
故答案为:二;ⅤA;
(2)E为S元素,对应的氧化物的水化物有H2SO3、H2SO4;
故答案为:H2SO3、H2SO4
(3)元素B、C、D、E形成的离子分别为N3-、O2-、Na+、S2-,S2-离子核外有3个电子层,离子半径最大,N3-,O2-与Na+离子核外电子排布相同,都有2个电子层,核电核数越大,离子半径越小,则离子半径N3->O2->Na+;
故答案为:S2->N3->O2->Na+;
(4)化合物D2C为Na2O,为离子化合物,用电子式表示的形成过程为 ;
;
故答案为: ;
;
(5)由A、B、C三种元素形成的盐为NH4NO3,加热条件下,与强碱溶液反应生成氨气,离子反应方程式为:
NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案为:NH4NO3;NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2↑
(6)D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,故反应的化学方程式为4Na2SO3=Na2S+3Na2SO4;
故答案为:4Na2SO3=Na2S+3Na2SO4;
(7)∵m(BaSO4)=mg
∴n(BaSO4)=$\frac{m}{233}$mol
根据硫原子守恒,则n(SOX)=n(BaSO4)=$\frac{m}{233}$mol
∴v(SOX)=nVm=$\frac{22.4m}{233}$L
∴W(SOX)=$\frac{22.4m}{233v}$
故答案为:$\frac{22.4m}{233v}$.
点评 本题考查元素位置结构性质的相互关系应用,题目难度中等,注意正确推断元素的种类为解答该题的关键,注意用电子式表示化学键或物质的形成.

| A. | 2mol | B. | 4mol | C. | 6mol | D. | 8mol |
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 在常温下,铝不能与浓硫酸反应 | |
| C. | 铝是一种比较活泼的金属 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
| A. | 该电池中Zn为负极,发生还原反应 | |
| B. | 该电池的正极反应式为MnO2+e-+H2O=MnOOH+OH- | |
| C. | 导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn | |
| D. | 电池工作时内电路中OH-移动向MnO2一极 |
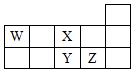
| A. | Z、Y、X的原子半径依次减小,非金属性依次降低 | |
| B. | Z、Y、W的最高价氧化物对应水化物的酸性依次降低 | |
| C. | WH4与Z元素的单质在一定条件下可能发生化学反应 | |
| D. | W的位置是第2周期、第ⅣA族 |
| A. | 氨水 | B. | 氢氧化钠 | C. | 氢氧化钡 | D. | 氢氧化钙 |