题目内容
18.室温下,下列有关0.1mol•L-1氨水的说法正确的是( )| A. | 溶液的pH>13 | |
| B. | 加水稀释,溶液中c(H+)和c(OH-)都减小 | |
| C. | 该溶液中:c(OH-)=c(NH4+) | |
| D. | 完全中和等物质的量的HCl,消耗的体积与0.1 mol•L-1NaOH溶液一样多 |
分析 氨水中存在NH3.H2O?OH-+NH4+,稀释促进电离,但Kw不变,且酸碱中和时n(HCl)=n(一元碱),以此来解答.
解答 解:A.一水合氨为弱碱,不能完全电离,则0.1mol•L-1氨水中氢氧根离子浓度小于0.1mol/L,则溶液的pH<13,故A错误;
B.加水稀释,溶液中c(OH-)减小,Kw不变,则c(H+)增大,故B错误;
C.由一水合氨电离及水的电离可知,该溶液中:c(OH-)>c(NH4+),故C错误;
D.酸碱中和时n(HCl)=n(一元碱),则完全中和等物质的量的HCl,消耗的体积与0.1 mol•L-1NaOH溶液一样多,故D正确;
故选D.
点评 本题考查弱电解质的电离平衡,为高频考点,把握电离平衡移动、酸碱混合为解答本题的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
8.银质器皿日久表面会逐渐变黑,这是生成了 Ag2S 的缘故.根据化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去.下列说正确的是( )
| A. | 过程中银器一直保持恒重 | |
| B. | 银器为正极,Ag2S 被还原生成单质银 | |
| C. | 铝质容器为正极 | |
| D. | 黑色褪去的原因是黑色 Ag2S 转化为白色 AgCl |
9.下列说法中,不正确的是( )
| A. | 油脂水解的产物中一定含甘油 | |
| B. | 糖类、油脂和蛋白质都属于高分子化合物 | |
| C. | 氨基酸既能与盐酸反应,也能与NaOH反应 | |
| D. | 医疗上用75%的酒精消毒是因为其能使蛋白质变性 |
6.标准状况下,将11.2L CO2缓缓通入300mL 2mol•L-1的NaOH溶液中,待充分反应后将所得溶液蒸干并充分灼烧,最后所得固体物质质量为( )
| A. | 31.8g | B. | 53g | C. | 63.6g | D. | 84g |
13.取a g CO在足量的O2中完全燃烧,将生成物与足量Na2O2固体完全反应,反应后,固体增加的质量为( )
| A. | 小于a g | B. | 等于a g | C. | 大于a g | D. | 无法确定 |
3.下列关于如图装置说法中正确的是( )
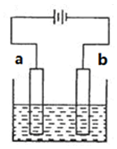

| A. | 精炼铜时,a极为粗铜,b极为精铜 | |
| B. | 电镀铜时,a极为镀件,b极为铜 | |
| C. | 保护铁时,a极为铁片,b极为锌片 | |
| D. | 惰性电极电解饱和食盐水时,b极有黄绿色气体产生 |
10.下列说法正确的是( )
| A. | 用于纺织的棉花和蚕丝的主要成分是纤维素 | |
| B. | 75%的乙醇溶液可用于医疗消毒,福尔马林可用于浸制动物标本,二者所含原理一样 | |
| C. | 食物中的淀粉类物质,通过人体中酶的催化作用下转化为酒精 | |
| D. | 向鸡蛋清的溶液中加入浓硫酸铜溶液,可观察到蛋白质发生凝聚,再加入蒸馏水,振荡后蛋白质又发生溶解 |