题目内容
12.如果1g水中含有a个氢原子,则阿伏加德罗常数是( )| A. | $\frac{1}{9a}$ mol-1 | B. | 9a mol-1 | C. | 2a mol-1 | D. | 18a mol-1 |
分析 依据阿伏加德罗常数的含义进行计算,利用题给物理量用质量求的原子物质的量与用微粒数计算的物质的量相同.
解答 解:阿伏伽德罗常数用NA表示,1g水的物质的量=$\frac{1g}{18g/mol}$,含氧原子物质的量=$\frac{1}{18}$mol,a个氧原子物质的量=$\frac{a}{{N}_{A}}$mol,依据氧原子物质的量相同得到$\frac{1}{18}$=$\frac{a}{{N}_{A}}$mol,得到NA=18a/mol.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
20.为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
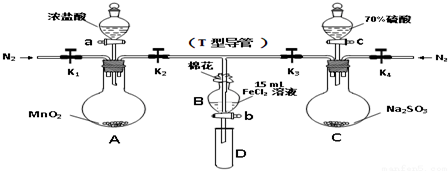
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A.
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子.
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子..
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)若向第Ⅲ步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式2Fe3++H2S═2Fe2++2H++S↓
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是甲(填“甲”“乙”“丙”)
(5)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入1.12LCl2(标准状况下),若溶液中有$\frac{1}{2}$的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为0.5mol/L.

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,加热A.
Ⅲ.当B中溶液变黄时,停止加热,夹紧K2.
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,并检验其中的离子.
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后夹紧K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子..
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)若向第Ⅲ步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式2Fe3++H2S═2Fe2++2H++S↓
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为2KMnO4+5SO2+2H2O=2MnSO4+K2SO4+2H2SO4
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是甲(填“甲”“乙”“丙”)
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
7.下列各说法正确的是( )
| A. | 弱电解质的导电能力一定比强电解质的导电能力弱 | |
| B. | pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液显碱性 | |
| C. | 豆浆中加入硫酸钙会使蛋白质聚沉. | |
| D. | 同浓度的①NaHCO3②Na2CO3③CH3COONa四种溶液,pH值大小排列顺序是②>①>③ |
4.下列说法不正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化不一定都是化学反应 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量总是大于生成物的总能量 |
11.只含非金属元素的晶体描述正确的是( )
| A. | 有可能是金属晶体 | B. | 有可能是离子晶体 | ||
| C. | 一定是分子晶体 | D. | 一定不是原子晶体 |
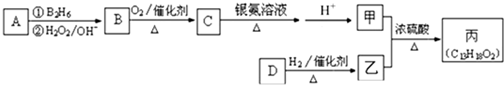
 -CH=CHCHO
-CH=CHCHO -CH2CH2CH2OH
-CH2CH2CH2OH (CH3)2CHCOOCH2CH2CH2-
(CH3)2CHCOOCH2CH2CH2- +H2O
+H2O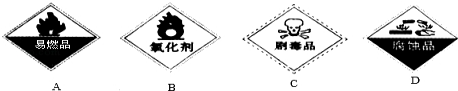
 .
.