题目内容
14.已知下列反应在1362K时的平衡常数:(1)H2(g)+$\frac{1}{2}$S2(g)?H2S(g) KΘ(1)=0.80
(2)3H2(g)+SO2(g)?2H2O(g)+H2S(g) KΘ(2)=1.8×104
计算反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)在该温度时的平衡常数KΘ.
分析 平衡常数为产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,写出每个反应的化学平衡常数表达式.
解答 解:平衡常数等于生成物浓度系数次幂之积除以反应物浓度系数次幂之积,
反应(1)H2(g)+$\frac{1}{2}$S2(g)?H2S(g)平衡常数K(1)=$\frac{c({H}_{2}S)}{c(H{\;}_{2}){c}^{\frac{1}{2}}(S{\;}_{2})}$,
反应(2)3H2(g)+SO2(g)?2H2O(g)+H2S(g)平衡常数K(2)=$\frac{c(H{\;}_{2}S){c}^{2}(H{\;}_{2}O)}{{c}^{3}(H{\;}_{2}){c}^{2}(S{O}_{2)}}$,
反应(3)4H2(g)+2SO2(g)?S2(g)+4H2O(g) 平衡常数K=$\frac{c(S{\;}_{2}){c}^{4}(H{\;}_{2}O)}{{c}^{4}(H{\;}_{2}){c}^{2}(SO{\;}_{2})}$,
反应2×(2)-2×(1)=反应(3),所以K=$\frac{{{K}^{2}}_{(2)}}{{{K}^{2}}_{(1)}}$=$\frac{(1.8×10{\;}^{4})^{2}}{0.80{\;}^{2}}$=5.06×108,
答:反应4H2(g)+2SO2(g)?S2(g)+4H2O(g)在该温度时的平衡常数KΘ 为5.06×108.
点评 本题考查化学平衡常数的意义,和平衡常数的书写、及综合应用,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.某有机物的结构简式为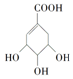 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )
 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )| A. | 该有机物能使溴的四氯化碳溶液褪色 | |
| B. | 该有机物发生消去反应可得到芳香烃 | |
| C. | 该有机物在一定条件下可发生氧化反应 | |
| D. | 1 mol该有机物最多可与1 mol NaHCO3反应 |
9.下列离子方程式表达正确的是( )
| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向漂白粉稀溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++SO42-+Ba2++4OH-═NH3•H2O+Al(OH)3↓+BaSO4↓ | |
| D. | 酸性溶液中KIO3与KI反应:I-+IO3-+6H+═I2+3H2O |
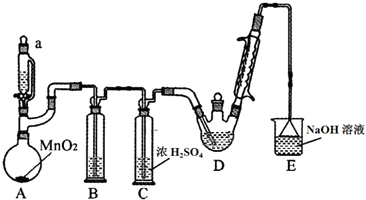
9.某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl,可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O;CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
(1)仪器a的名称是恒压分液漏斗,球形冷凝管的水流方向是下口进上口出.
(2)装置B中的试剂是饱和食盐水,若撤去装置B,可能导致装置D中副产物CCl3COOH、C2H5Cl(填化学式)的量增加.
(3)写出E中所有可能发生的无机反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行及其原因不可行,三氯乙酸可溶于乙醇、三氯乙醛.
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol/LNa2S2O3溶液滴定至终点.进行三次平行实验,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为66.4%.(计算结果保留三位有效数字)
滴定的反应原理:CCl3CHO+OH-=CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是ABC
A.分别测定0.1mol/L两种酸溶液的pH,三氯乙酸的pH较小
B.用仪器测量浓度均为0.1mol/L的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
C.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大.

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl,可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O;CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的相对分子质量及部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水,乙醇 | 可溶于水,乙醇,三氯乙醛 | 微溶于水,可溶于乙醇 |
(2)装置B中的试剂是饱和食盐水,若撤去装置B,可能导致装置D中副产物CCl3COOH、C2H5Cl(填化学式)的量增加.
(3)写出E中所有可能发生的无机反应的离子方程式Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(4)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行及其原因不可行,三氯乙酸可溶于乙醇、三氯乙醛.
(5)测定产品纯度:称取产品0.40g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol/LNa2S2O3溶液滴定至终点.进行三次平行实验,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为66.4%.(计算结果保留三位有效数字)
滴定的反应原理:CCl3CHO+OH-=CHCl3+HCOO-;HCOO-+I2=H++2I-+CO2↑;I2+2S2O32-═2I-+S4O62-
(6)为证明三氯乙酸的酸性比乙酸强,某学习小组的同学设计了以下三种方案,你认为能够达到实验目的是ABC
A.分别测定0.1mol/L两种酸溶液的pH,三氯乙酸的pH较小
B.用仪器测量浓度均为0.1mol/L的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
C.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH较大.
10.在某些火箭发射中常用肼(N2H4)为燃料.0.1mol N2H4(气态)在O2(气态)中燃烧生成N2(气态)和H2O(气态),放出53.4kJ的热量,则下列热化学方程式正确的是( )
| A. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=+534 kJ•L-1 | |
| B. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=-53.4 kJ•L-1 | |
| C. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=+53.4 kJ•L-1 | |
| D. | N2H4(g)+2O2(g)═N2(g)+2H2O(g);△H=-534 kJ•L-1 |