题目内容
9.下列离子方程式表达正确的是( )| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向漂白粉稀溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++SO42-+Ba2++4OH-═NH3•H2O+Al(OH)3↓+BaSO4↓ | |
| D. | 酸性溶液中KIO3与KI反应:I-+IO3-+6H+═I2+3H2O |
分析 A.反应生成氢氧化铝和硫酸铵;
B.反应生成碳酸氢钙、HClO;
C.使SO42-完全沉淀,反应生成硫酸钡、氢氧化铝和一水合氨,不符合离子的配比;
D.电子、电荷不守恒.
解答 解:A.向Al2(SO4)3溶液中加入过量氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A错误;
B.向漂白粉稀溶液中通入过量CO2的离子反应为ClO-+CO2+H2O═HClO+HCO3-,故B正确;
C.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀的离子反应为NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓,故C错误;
D.酸性溶液中KIO3与KI反应的离子反应为5I-+IO3-+6H+═3I2+3H2O,故D错误;
故选B.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意复分解反应及氧化还原反应的判断,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
17.25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | 在0.1 mol•L-1Na2S溶液中:2c(Na+)>c(S2-)>c(HS-)>c(OH-) | |
| B. | 一定量的(NH4)2SO4与NH3•H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) | |
| C. | 将0.1 mol•L-1盐酸与0.1 mol•L-1K2CO3溶液等体积混合:c(K+)>c(Cl-)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | 将0.1 mol•L-1Na2CO3溶液和0.1 mol•L-1NaHCO3溶液等体积混合:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
7.某温度时,N2+3H2?2NH3的平衡常数K=a,则此温度下,NH3?$\frac{3}{2}$H2+$\frac{1}{2}$N2的平衡常数为( )
| A. | $\frac{1}{\sqrt{a}}$ | B. | $\sqrt{a}$ | C. | $\frac{1}{2}$a | D. | $\frac{1}{\frac{1}{2}a}$ |
5.N2O4(无色)?2NO2(红综色),其能量变化示意图如下,则关于该反应的说法正确的是( )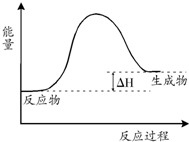

| A. | 该反应是吸热反应 | |
| B. | 当反应达到平衡时,升高温度,混合气体的颜色变浅 | |
| C. | 反应体系中加入催化剂对反应热是有影响 | |
| D. | 在反应体系中加入催化剂,正反应速率增大,逆反应速率减小 |