题目内容
7.向甲烷与丙炔的混合气体中加入一氧化碳气体,不论加入一氧化碳的体积如何改变,混合气体的密度始终不会改变(同温同压),则甲烷与丙炔的体积比是( )| A. | 1:1 | B. | 4:3 | C. | 3:2 | D. | 3:4 |
分析 向甲烷与丙炔的混合气体中加入一氧化碳气体,不论加入一氧化碳的体积如何改变,混合气体的密度始终不会改变(同温同压),则说明甲烷和丙炔混合气的密度与同温同压下一氧化碳的密度相同,则甲烷与丙炔混合气体的平均相对分子质量与CO相等为28,设甲烷的体积分数为x,则丙炔的体积分数为1-x,根据平均相对分子质量列方程计算,据此解答.
解答 解:向甲烷与丙炔的混合气体中加入一氧化碳气体,不论加入一氧化碳的体积如何改变,混合气体的密度始终不会改变(同温同压),则说明甲烷和丙炔混合气的密度与同温同压下一氧化碳的密度相同,则甲烷与丙炔混合气体的平均相对分子质量与乙烷相等为28,
设甲烷的体积分数为x,则丙炔的体积分数为1-x,
16x+40(1-x)=28,
解得:x=0.5,
故混合气中甲烷和丙烷的体积比为x:(1-x)=0.5:(1-0.5)=1:1,
故选A.
点评 本题考查混合物的有关计算、阿伏伽德罗定律及推论的应用,题目难度不大,理解平均相对分子质量的计算是关键,注意掌握密度与摩尔质量之间的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.如图表示M的结构简式,下列有关M的说法正确的是( )
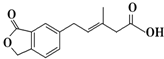

| A. | M可以发生加成、加聚、水解、酯化等反应 | |
| B. | 1mol M最多可以与3mol NaOH反应 | |
| C. | M苯环上的一氯取代物有三种不同结构 | |
| D. | 1mol M最多可以与5mol H2发生加成反应 |
18.下列说法不正确的是( )
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 | |
| C. | 同系物的分子量数值一定相差14的整数倍 | |
| D. | 同系物的化学性质相似,物理性质随碳原子数的递增呈现规律性变化 |
15.下列不能用于金属防腐处理的是( )
| A. | 涂油漆 | |
| B. | 海轮在海洋上航行,为防止船体腐蚀,常在船体上镶上铜块 | |
| C. | 在金属表面进行电镀 | |
| D. | 改变金属内部结构 |
2.下列有关晶体的说法正确的是( )
| A. | 任何晶体中都存在化学键 | |
| B. | 固体SiO2一定是晶体 | |
| C. | 晶体的自范性是晶体中粒子在微观空间里呈现周期性的有序排列的宏观表象 | |
| D. | X-射线衍射法是区分晶体和非晶体的唯一方法 |
12.600K时,庚烷发生反应C7H16(g)$\stackrel{△}{→}$CmHn(g)+CpHq(g)+CxHy(g)(已配平),测得反应前后容器内压强分别是1.01×105Pa和2.02×105Pa(均在600K测定),则庚烷的分解率为( )
| A. | 20% | B. | 50% | C. | 66.7% | D. | 80% |
19.X、Y、Z是原子序数依次增大的短周期元素,3种元素的原子核外电子数之和与Ar的核外电子数相等,X、Z的-1价简单离子与同周期稀有气体原子具有相同的电子层结构.下列说法正确的是( )
| A. | Z的气态氢化物稳定性强于其它的非金属气态氢化物 | |
| B. | 原子半径:Z>Y>X | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | CaX2、CaY2和CaZ23种化合物中,阳离子与阴离子个数比均为1:2 |
16.下列各组离子在指定条件下,能大量共存的是( )
| A. | 碱性溶液中:Rb+、Cs+、CH3COO-、Br- | B. | 饱和溴水中 I-、NO3-、Na+、SO32- | ||
| C. | D+、Cl-、NO3-、SiO32- | D. | Ag+、Fe3+、Br-、SO42- |
17.在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量成为键能(kJ•mol-1).下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
(1)根据上表中的数据判断工业合成氨的反应是放热(填“吸热”或“放热”)反应;
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应. 理论上放出或吸收的热量为Q1,则Q1为93KJ.
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是B
A.Q1>Q2B.Q1<Q2 C.Q1=Q2.
| 共价键 | H2分子 | N2分子 | NH3分子 |
| 键能(KJ•mo1-1) | 436 | 945 | 391 |
(2)在298K时,取1mol氮气和3mol氢气放入一密闭容器中,在催化剂存在下进行反应. 理论上放出或吸收的热量为Q1,则Q1为93KJ.
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是B
A.Q1>Q2B.Q1<Q2 C.Q1=Q2.