题目内容
16.下列各组离子在指定条件下,能大量共存的是( )| A. | 碱性溶液中:Rb+、Cs+、CH3COO-、Br- | B. | 饱和溴水中 I-、NO3-、Na+、SO32- | ||
| C. | D+、Cl-、NO3-、SiO32- | D. | Ag+、Fe3+、Br-、SO42- |
分析 A.碱性溶液中,该组离子之间不反应;
B.溴水具有氧化性,不能存在还原性离子;
C.离子之间结合生成沉淀;
D.离子之间结合生成沉淀.
解答 解:A.碱性溶液中,该组离子之间不反应,可大量共存,故A错误;
B.溴水具有氧化性,与I-、SO32-发生氧化还原反应,或NO3-、I-(或SO32-)发生氧化还原反应,不能共存,故B错误;
C.D+、SiO32-结合生成沉淀,不能共存,故C错误;
D.Ag+分别与Br-、SO42-结合生成沉淀,不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应及离子的颜色为解答的关键,侧重复分解反应、氧化还原反应的离子共存及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.下列有关物质的性质与其应用不相对应的是( )
| A. | MgO、Al2O3的熔点很高,可制作耐高温材料 | |
| B. | 新制氯水久置后变为无色 | |
| C. | 单质硅是光导纤维的主要成分 | |
| D. | 普通玻璃导管口点燃纯净氢气时,火焰呈黄色 |
7.向甲烷与丙炔的混合气体中加入一氧化碳气体,不论加入一氧化碳的体积如何改变,混合气体的密度始终不会改变(同温同压),则甲烷与丙炔的体积比是( )
| A. | 1:1 | B. | 4:3 | C. | 3:2 | D. | 3:4 |
4.对于苯乙烯(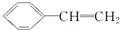 )有下列叙述:
)有下列叙述:
①能使酸性KMnO4溶液褪色;
②能使溴的四氯化碳溶液褪色;
③可溶于水;
④可溶于苯中;
⑤能与浓硝酸发生取代反应;
⑥所有的原子一定共平面.
其中正确的是( )
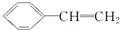 )有下列叙述:
)有下列叙述:①能使酸性KMnO4溶液褪色;
②能使溴的四氯化碳溶液褪色;
③可溶于水;
④可溶于苯中;
⑤能与浓硝酸发生取代反应;
⑥所有的原子一定共平面.
其中正确的是( )
| A. | ①②③④⑤ | B. | ①②⑤⑥ | C. | ①②④⑤⑥ | D. | ①②④⑤ |
11.下列说法一定错误的是( )
| A. | Se是人体必需的微量元素,${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素,是两种不同的核素 | |
| B. | 某些花岗石产生氡(${\;}_{86}^{222}$Rn),从而对人体产生伤害,Rn元素的相对原子质量是222 | |
| C. | ${\;}_{92}^{235}$U的浓缩一直被国际社会关注,其中子数和质子数之差为51 | |
| D. | 112号元素属于过渡元素 |
1.下列各组物质的性质,从左到右依次递减的是( )
| A. | 碱性:Al(OH)3、Mg(OH)2、NaOH | B. | 酸性:HClO4、H2SO4、H3PO4 | ||
| C. | 还原性:HCl、HBr、HI | D. | 原子半径:S、Na、O |
5.下列实验装置与目的不相符的是( )
| A. | 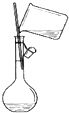 向容量瓶中转移液体 | B. |  蒸干NH4Cl饱和溶液制备NH4Cl晶体 | ||
| C. | 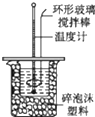 中和热的测定 | D. |  分离四氯化碳和水 |
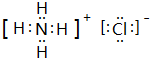 ,化学键类型有离子键、极性键(填“离子键”“极性键”或“非极性键”).
,化学键类型有离子键、极性键(填“离子键”“极性键”或“非极性键”).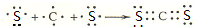 .
. .
.