题目内容
7.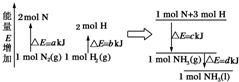 化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
分析 根据反应热等于反应物总能量减去生成物总能量计算反应热并书写热化学方程式,注意反应物的物质的量和生成物的聚集状态.
解答 解:由图可以看出,molN2(g)+$\frac{3}{2}$molH2(g)的能量为akJ,1molNH3(g)的能量为bkJ,
所以 $\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(a-b)kJ/mol,
而1mol的NH3(g)转化为1mol的NH3(l)放出的热量为ckJ,
所以有:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(l)△H=(a-b-c)kJ/mol,
即:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
故答案为:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
点评 本题考查反应热与能量变化,侧重于考查学生的分析能力和自学能力,题目难度不大,注意把握题给信息,答题时注意仔细审题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.等质量的下列有机物完全燃烧时耗氧量最大的是( )
| A. | C2H6 | B. | C3H4 | C. | C6H6 | D. | C2H4 |
15.表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~(3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答.
(1)写出金属性最强元素与水的方应的方程式:2Na+2H20=2NaOH+H2↑.
(2)A分别与D、E、G、形成的化合物中,稳定性由弱到强的顺序:CH4<NH3<HF,
(3)F、H元素对应的最高价氧化物含氧酸由强到弱的顺序是:H3PO4<HClO4,
(4)A和E组成化合物比A和F组成化合物的沸点高(填“高”或“低”),原因是氨气分子间存在氢键
(5)用电子式表示B的最高价氧化物对应的水化物的形成过程
(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式Al2O3+2OH-═2AlO2-+H2O.
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)A分别与D、E、G、形成的化合物中,稳定性由弱到强的顺序:CH4<NH3<HF,
(3)F、H元素对应的最高价氧化物含氧酸由强到弱的顺序是:H3PO4<HClO4,
(4)A和E组成化合物比A和F组成化合物的沸点高(填“高”或“低”),原因是氨气分子间存在氢键
(5)用电子式表示B的最高价氧化物对应的水化物的形成过程

(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式Al2O3+2OH-═2AlO2-+H2O.
12.某原电池总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的正确组成是( )
| A | B | C | D | |
| 正极 | Zn | Cu | Cu | Fe |
| 负极 | Cu | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | AgNO3 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
19.四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)元素Z位于周期表中第三周期,VA族;
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)Y的最高价氧化物的化学式为N2O5.
请回答下列问题:
| X | Y | |
| Z | W |
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)Y的最高价氧化物的化学式为N2O5.
16.表是元素周期表的一部分.
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)画出原子结构示意图:⑪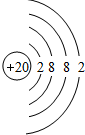 .
.
(5)用电子式表示⑦和⑩形成化合物的过程: .
.
(6)⑦和⑧分别形成的气态氢化物的化学式是H2S、HCl.其中相对不稳定的是H2S.
(7)在③与④中,化学性质较活泼的是Na(填元素符号),在⑧与⑫中,化学性质较活泼的是Cl,(填元素符号)如何证明(用离子方程式表示):Cl2+2Br-═Br2+2Cl-.
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出下列元素符号:①N,⑥Si.
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.(用化学式填写)
(3)在这些元素中单质的氧化性最强的是F2,还原性最强的是K.化学性质最不活泼的元素是Ar.(用化学式填写)
(4)画出原子结构示意图:⑪
 .
.(5)用电子式表示⑦和⑩形成化合物的过程:
 .
.(6)⑦和⑧分别形成的气态氢化物的化学式是H2S、HCl.其中相对不稳定的是H2S.
(7)在③与④中,化学性质较活泼的是Na(填元素符号),在⑧与⑫中,化学性质较活泼的是Cl,(填元素符号)如何证明(用离子方程式表示):Cl2+2Br-═Br2+2Cl-.
17.下列有关硅及其化合物的叙述中,错误的是( )
| A. | 单质硅是良好的半导体材料 | B. | 硅常温时可以和强碱反应 | ||
| C. | 二氧化硅广泛存在于自然界 | D. | 硅酸是挥发性酸 |