题目内容
17.下列有关硅及其化合物的叙述中,错误的是( )| A. | 单质硅是良好的半导体材料 | B. | 硅常温时可以和强碱反应 | ||
| C. | 二氧化硅广泛存在于自然界 | D. | 硅酸是挥发性酸 |
分析 A.硅的导电性介于导体与绝缘体之间;
B.硅常温下能与强碱反应生成硅酸盐和氢气;
C.自然界中无游离态硅,硅是亲氧元素,硅在自然界中以化合态存在;
D.根据硅酸的性质分析.
解答 解:A.硅的导电性介于导体与绝缘体之间是良好的半导体材料,故A正确;
B.硅常温下能与强碱反应生成硅酸盐和氢气,故B正确;
C.硅在自然界中以二氧化硅和硅酸盐的形式存在,故C正确;
D.硅酸是固体酸、弱酸,易分解,但不易挥发,故D错误;
故选:D.
点评 本题主要考查了硅及含硅化合物,侧重于常识性内容的考查,难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
| A. | 10℃20mL 3mol/L的X溶液 | B. | 20℃30mL 2molL的X溶液 | ||
| C. | 20℃10mL 4mol/L的X溶液 | D. | 10℃10mL 2mol/L的X溶液 |
5.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
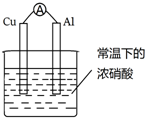

| A. | 电子由Al沿导线流向Cu | |
| B. | 电流由Cu电极流出 | |
| C. | Cu是原电池的负极 | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
2.下列各物质中,化学键类型不同的是( )
| A. | H2O、CO | B. | MgF2、H2O2 | C. | KOH、Mg(OH)2 | D. | HCl、H2SO4 |
9.一定温度下,对反应2A(g)+B(s)?2C(g)能说明其达到平衡状态的是( )
| A. | 容积中A、B、C三者共存 | |
| B. | 单位时间内反应的A与生成的C的物质的量之比为1:1 | |
| C. | c(A):c(B):c(C)=2:1:2 | |
| D. | 气体的总质量不再发生变化 |
6.下列比较正确的是( )
| A. | 元素的电负性:S>P | B. | 晶体的硬度:碳化硅<晶体硅 | ||
| C. | 酸性:H3PO4<H3PO3 | D. | 热分解温度:CaCO3>BaCO3 |
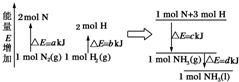 化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1. ;
;