题目内容
12.某原电池总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的正确组成是( )| A | B | C | D | |
| 正极 | Zn | Cu | Cu | Fe |
| 负极 | Cu | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | AgNO3 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
分析 由电池反应式Zn+Cu2+═Zn2++Cu知,锌失电子发生氧化反应,作负极;不如锌活泼的金属或导电的非金属作正极,正极上铜离子得电子发生还原反应,则电解质溶液中应含有铜离子,所以应为可溶性的铜盐.
解答 解:由电池反应式Zn+Cu2+═Zn2++Cu知,锌失电子发生氧化反应,作负极;不如锌活泼的金属或导电的非金属作正极,正极上铜离子得电子发生还原反应,则电解质溶液中应含有铜离子,所以应为可溶性的铜盐,
A、锌应作负极,铜作正极,故A错误;
B、该装置中,锌易失电子作负极,铜作正极,电解质溶液不含可溶性的铜盐,不符合条件,故B错误;
C、电解质不含铜离子的盐溶液,故C错误;
D.该装置中,锌易失电子作负极,铁作正极,电解质溶液为可溶性的铜盐,故D正确.
故选D.
点评 本题考查了原电池原理,难度不大,明确原电池的构成条件是解本题关键,注意根据方程式中发生的反应类型判断原电池的正负极及电解质溶液.

练习册系列答案
相关题目
11.已知某元素的阳离子R2+的核内中子数为n,质量数为A,则mg它的氧化物中所含电子的物质的量是( )
| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A}$(A-n+6)mol |
3.如图所示是气体性质实验的常用装置,下列有关实验现象的说法不正确的是( )
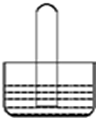

| A. | 若水槽中是水,试管中是NO2,可看到液面上升并且气体颜色逐渐变浅 | |
| B. | 若水槽中是NaOH溶液,试管中是Cl2,可看到液面上升、试管中黄绿色褪去 | |
| C. | 若水槽中是水并滴有几滴紫色石蕊,试管中是SO2,可看到液面上升并变为无色 | |
| D. | 若水槽中是水并滴有几滴酚酞,试管中是NH3,可看到液面上升并呈红色 |
20.某密闭容器中,有下列反应发生:A(g)+3B(g)?2C(g)+D(g).若0-2min时间段内v(A)=1mol/(L•min),则此段时间v(C)为( )
| A. | 0.5 mol/(L•min) | B. | 1 mol/(L•min) | C. | 2 mol/(L•min) | D. | 3 mol/(L•min) |
4.下列有关功能高分子材料的用途的叙述中不正确的是( )
| A. | 高吸水性树脂可用于干旱地区抗旱保水、改良土壤、改造沙漠 | |
| B. | 离子交换树脂主要用于分离和提纯物质 | |
| C. | 医用高分子可用于制造医用器械和人造器官 | |
| D. | 聚乙炔膜可用于分离工业废水和海水的淡化 |
1.按官能团分类,下列说法正确的是( )
| A. | 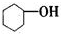 属于芳香族化合物 属于芳香族化合物 | B. |  属于羧酸 属于羧酸 | ||
| C. |  属于醛类 属于醛类 | D. |  属于酚类 属于酚类 |
2.下列各物质中,化学键类型不同的是( )
| A. | H2O、CO | B. | MgF2、H2O2 | C. | KOH、Mg(OH)2 | D. | HCl、H2SO4 |
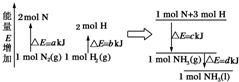 化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.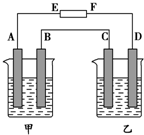 如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则
如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则