题目内容
19.四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.请回答下列问题:
| X | Y | |
| Z | W |
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)Y的最高价氧化物的化学式为N2O5.
分析 短周期元素,Z元素原子的核外电子总数是其最外层电子数的3倍,设最外层为x,则(2+8+x)=3x,解得x=5,则Z为P;然后由元素周期表中的位置可知,X为C,Y为N,W为S,然后依据元素及其单质、化合物的性质来解答.
解答 解:短周期元素,Z元素原子的核外电子总数是其最外层电子数的3倍,设最外层为x,则(2+8+x)=3x,解得x=5,则Z为P;然后由元素周期表中的位置可知,X为C,Y为N,W为S,
(1)Z为P,原子结构中有3个电子层,最外层电子数为5,则位于元素周期表中的第三周期,第VA族,故答案为:三;VA;
(2)上述元素的氢化物中,氨气的水溶液碱性最强,氨气的化学式为NH3,故答案为:NH3;
(3)Y为N,N的最高价为+5价,则最高价氧化物的化学式为N2O5,故答案为:N2O5.
点评 本题考查位置、结构与性质的综合应用,为高频考点,把握元素的位置、元素周期律、元素化合物知识为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
10.下列反应的离子方程式正确的是( )
| A. | 氨气通入盐酸溶液 HCl+NH3═NH4Cl | |
| B. | 澄清的石灰水跟盐酸反应 H++OH-═H2O | |
| C. | 碳酸钡溶于醋酸 BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 金属钠跟水反应 Na+2H2O═Na++2OH-+H2↑ |
4.下列有关功能高分子材料的用途的叙述中不正确的是( )
| A. | 高吸水性树脂可用于干旱地区抗旱保水、改良土壤、改造沙漠 | |
| B. | 离子交换树脂主要用于分离和提纯物质 | |
| C. | 医用高分子可用于制造医用器械和人造器官 | |
| D. | 聚乙炔膜可用于分离工业废水和海水的淡化 |
11.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是( )
| A. | 金属性:Y>Z | B. | 氢化物的稳定性:X>W | ||
| C. | 离子的还原性:X>W | D. | 离子半径:Z>Y>X |
8.下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
| A. | 10℃20mL 3mol/L的X溶液 | B. | 20℃30mL 2molL的X溶液 | ||
| C. | 20℃10mL 4mol/L的X溶液 | D. | 10℃10mL 2mol/L的X溶液 |
9.一定温度下,对反应2A(g)+B(s)?2C(g)能说明其达到平衡状态的是( )
| A. | 容积中A、B、C三者共存 | |
| B. | 单位时间内反应的A与生成的C的物质的量之比为1:1 | |
| C. | c(A):c(B):c(C)=2:1:2 | |
| D. | 气体的总质量不再发生变化 |
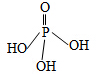 (1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为
(1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为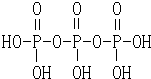 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.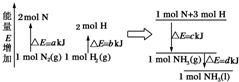 化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.