题目内容
2.把0.6molX、0.4molY混合后,在2L密闭容器中发生反应:3X(g)+Y(g)═nZ(g)+2W(g),5min末已生成0.2molW,并测得这段时间内v(Z)=0.01mol/(L•min).上述反应中Z的化学计量数n是( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 根据△n=v×△t×V计算生成n(Z),再根据物质的量之比等于化学计量数之比计算.
解答 解:生成Z的物质的量为5min×0.01mol/(L•min)×2L=0.1mol,
物质的量之比等于化学计量数之比,则n:2=0.1mol:0.2mol,故n=1,
故选:A.
点评 本题考查化学反应速率有关计算,比较基础,注意对速率公式的理解与灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列说法中不正确的是( )
| A. | 将化学能转变为电能的装置叫做原电池 | |
| B. | 乙醇和沼气都是可再生能源 | |
| C. | CO2是造成酸雨的主要原因之一 | |
| D. | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 |
10.下列反应的离子方程式正确的是( )
| A. | 氨气通入盐酸溶液 HCl+NH3═NH4Cl | |
| B. | 澄清的石灰水跟盐酸反应 H++OH-═H2O | |
| C. | 碳酸钡溶于醋酸 BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 金属钠跟水反应 Na+2H2O═Na++2OH-+H2↑ |
11.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是( )
| A. | 金属性:Y>Z | B. | 氢化物的稳定性:X>W | ||
| C. | 离子的还原性:X>W | D. | 离子半径:Z>Y>X |
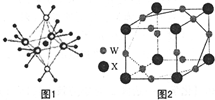 现有A、X、Y、Z、W五种元素,它们的原子序数依次增大.A原子的核外总数与其周期数相同;X基态原子的L电子层中有3个未成对电子;Y基态原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;Z基态原子的3p轨道上得到两个电子后不能再容纳外来电子;W基态原子的最外层电子数为1,其余各电子层均充电子层均充满电子.请回答下列问题:
现有A、X、Y、Z、W五种元素,它们的原子序数依次增大.A原子的核外总数与其周期数相同;X基态原子的L电子层中有3个未成对电子;Y基态原子的2p轨道上有一个电子的自旋方向与2p轨道上其他电子的自旋方向相反;Z基态原子的3p轨道上得到两个电子后不能再容纳外来电子;W基态原子的最外层电子数为1,其余各电子层均充电子层均充满电子.请回答下列问题: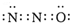 ,其中心原子的杂化轨道类型是sp,1molX2Y含有的π键数目为2NA.
,其中心原子的杂化轨道类型是sp,1molX2Y含有的π键数目为2NA.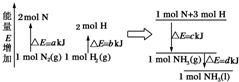 化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1.
化学反应N2(g)+3H2(g)=2NH3(l)的能量变化如图所示,(注:图中△E都为正值),写出该反应的热化学方程式:N2(g)+3H2(g)=2NH3(1)△H=2(a-b-c)kJ•mol-1. ;
;