题目内容
15.某校化学实验兴趣小组在“探究物质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色.(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致.则溶液呈黄色是含Br2(填化学式或离子符号,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
A.酚酞试液 B.四氯化碳 C.无水酒精 D.硫氰化钾溶液
请写出丙同学的一种方案,选用的试剂及实验现象填在下表空格中.(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案 | ①d或b | ②溶液变成血红色或下层的四氯化碳溶液依然无色 |
①在少量FeBr2溶液中通入足量Cl2,反应的离子方程式为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有$\frac{1}{3}$的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为1.2mol/L.
分析 (2)①根据溴水的颜色来进行猜想;
②根据发生氧化还原反应生成Fe3+及Fe3+在水中的颜色来猜想;
(3)利用Fe3+的检验及萃取来进行实验的设计,Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶;
(4)①由氧化性Br2>Fe3+,则氯化亚铁溶液中加入1~2滴溴水发生氧化还原反应生成Fe3+;
②根据电子守恒进行计算.
解答 解:(2)①因溴水的颜色为黄色,则溶液呈黄色是因为含有Br2所致,
故答案为:Br2;
②氧化性:Br2>Fe3+,则发生2Fe2++Br2=2Fe3++2Br-,生成Fe3+且Fe3+在水中为黄色,溶液呈黄色是因为含有Fe3+所致,
故答案为:Fe3+;
(3)因Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶,则
| 试剂 | 实验现象 | |
| 方案1 | d | 溶液变成血红色 |
| 方案2 | b | 下层的四氯化碳溶液依然无色 |
| 试剂 | 实验现象 | |
| 方案1 | d | 溶液变成血红色 |
| 方案2 | b | 下层的四氯化碳溶液依然无色 |
(4)①由还原性Br-<Fe2+,在少量FeBr2溶液中通入足量Cl2,亚铁离子和溴离子全部被氧化,反应的离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,
故答案为:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-;
②设FeBr2的物质的量浓度为c,
由电子守恒可知,$\frac{2.24L}{22.4L/mol}$×2×1=c×0.1L×(3-2)+c×0.1L×2×$\frac{1}{3}$×(1-0),
解得c=1.2mol/L,
故答案为:1.2mol/L.
点评 本题考查氧化还原反应及氧化性、还原性的比较、实验设计,学生应注意物质的性质及氧化还原反应中电子守恒来分析,题目难度中等.

练习册系列答案
相关题目
4.在某100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.4mol•L-1、0.1mol•L-1,向该混合液中加入1.92g铜粉,加热,待充分反应后,所得溶液中铜离子物质的量浓度( mol•L-1)是( )
| A. | 0.015 | B. | 0.225 | C. | 0.035 | D. | 0.045 |
3.已知A(g)+B(g)?C(g)+D(g)反应的平衡常数和温度的关系如下:
请回答下列问题:
(1)该反应平衡常数表达式为K=$\frac{c(C)•c(D)}{c(A)•c(B)}$;△H<0(选填“>”、“<”或“=”).
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,若测得反应初始至6S内A的平均反应速率v(A)=0.002mol•L-1•S-1,则6S时c(A)=0.028 mol•L-1;C的物质的量为0.06mol.
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为80%;保持温度、容器不变,再向密闭容器中充入0.20mol的A和0.80mol的B,此时A的转化率为80%;如果这时向该密闭容器中再充入1mol氩气,则平衡时A的转化率不变(选填“增大”、“减小”、“不变”).
(4)判断该反应是否达到平衡的依据为ce(填正确选项的字母).
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
e.单位时间内生成amolA的同时,消耗amolB
(5)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为2.5.
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应平衡常数表达式为K=$\frac{c(C)•c(D)}{c(A)•c(B)}$;△H<0(选填“>”、“<”或“=”).
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,若测得反应初始至6S内A的平均反应速率v(A)=0.002mol•L-1•S-1,则6S时c(A)=0.028 mol•L-1;C的物质的量为0.06mol.
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为80%;保持温度、容器不变,再向密闭容器中充入0.20mol的A和0.80mol的B,此时A的转化率为80%;如果这时向该密闭容器中再充入1mol氩气,则平衡时A的转化率不变(选填“增大”、“减小”、“不变”).
(4)判断该反应是否达到平衡的依据为ce(填正确选项的字母).
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
e.单位时间内生成amolA的同时,消耗amolB
(5)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为2.5.
10.A、B、D、E、F为短周期元素.非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍.B在D中充分燃烧能生成其最高价化合物BD2.E+与D2-具有相同的电子数.A在F中燃烧,产物溶于水得到一种强酸.回答下列问题:
(1)写出工业制备单质F的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其水溶液与F单质反应的化学方程式为2Na2CO3+Cl2+H2O═NaCl+NaClO+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如下表:
a的化学式为NaH;b的化学式为Na2O2;c的电子式为 ;d的晶体类型是金属.
;d的晶体类型是金属.
(1)写出工业制备单质F的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)B、D、E组成的一种盐中,E的质量分数为43%,其水溶液与F单质反应的化学方程式为2Na2CO3+Cl2+H2O═NaCl+NaClO+2NaHCO3.
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 ;d的晶体类型是金属.
;d的晶体类型是金属. 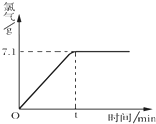 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与时间的关系如图所示.请计算:
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与时间的关系如图所示.请计算:
 .
.