题目内容
7.室温下将6g CH3COOH溶于水配制成1L的溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)浓度为1.4×10-3mol/L,此温度下醋酸的电离平衡常数K=1.96×10-5,此时溶液中由水电离出的c(H+)与c(OH-)之积小于(填“大于”、“小于”或“等于”)1.0×l0-14.温度升高,K将变大(填“变大”或“变小”或“不变”),醋酸的电离平衡向右移动(填“左”或“右”或“不”).分析 n(CH3COOH)=$\frac{6g}{60g/mol}$=0.1mol,根据c=$\frac{n}{V}$计算物质的量浓度;
根据k=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)}$计算电离平衡常数,结合外界条件对弱电解质的电离平衡的影响判断电离度的变化,酸碱抑制水的电离,
温度不变,平衡常数、离子积常数不变,升温促进弱电解质电离.
解答 解:n(CH3COOH)=$\frac{6g}{60g/mol}$=0.1mol,
c(CH3COOH)=$\frac{0.1mol}{1L}$=0.1mol/L,
k=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{1.4×1{0}^{-3}×1.4×1{0}^{-3}}{0.1-1.4×1{0}^{-3}}$=1.96×10-5,
醋酸抑制水的电离,溶液中由水电离出的c(H+)与c(OH-)之积小于1.0×l0-14,
醋酸的电离平衡常数只受温度的影响,醋酸电离过程为吸热过程,温度升高,醋酸电离平衡正向进行,平衡常数变大,
故答案为:0.1mol/L,1.96×10-5,小于,变大,右.
点评 本题考查弱电解质的电离,题目难度不大,本题注意把握弱电解质的电离特点,根据相关计算公式计算,注意电离度和电离平衡常数的区别.

练习册系列答案
相关题目
16.根据表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述中正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A. | 最高价氧化物对应水化物的碱性A<C | |
| B. | 氢化物的稳定性H2D<H2E | |
| C. | 单质与稀盐酸反应的速率A<B | |
| D. | C2+与A+的核外电子数相等 |
17.下列说法正确的是( )
| A. | 反应C(s)+H2O(g)═CO(g)+H2(g)的△H>0,△S>0 | |
| B. | 铅酸蓄电池放电时,负极质量减少,正极质量增加 | |
| C. | 向Na2S溶液中加入少量NaOH固体后,溶液中c(Na+)/c(S2- )减少 | |
| D. | 向平衡体系CH3COOH+C2H5OH?CH3COOC2H5+H2O中,加少量浓硫酸,乙酸转化率不变 |
15.某校化学实验兴趣小组在“探究物质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致.则溶液呈黄色是含Br2(填化学式或离子符号,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
A.酚酞试液 B.四氯化碳 C.无水酒精 D.硫氰化钾溶液
请写出丙同学的一种方案,选用的试剂及实验现象填在下表空格中.(试剂填序号)
(4)应用与拓展
①在少量FeBr2溶液中通入足量Cl2,反应的离子方程式为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有$\frac{1}{3}$的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为1.2mol/L.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致.则溶液呈黄色是含Br2(填化学式或离子符号,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含Fe3+所致.
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
A.酚酞试液 B.四氯化碳 C.无水酒精 D.硫氰化钾溶液
请写出丙同学的一种方案,选用的试剂及实验现象填在下表空格中.(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案 | ①d或b | ②溶液变成血红色或下层的四氯化碳溶液依然无色 |
①在少量FeBr2溶液中通入足量Cl2,反应的离子方程式为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有$\frac{1}{3}$的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为1.2mol/L.
19.下列说法中一定正确的是( )
| A. | Na2O2固体中阳离子与阴离子的个数比为1:1 | |
| B. | 从试剂瓶中取出并切下的未使用的钠可放回原试剂瓶中 | |
| C. | 将Na投入饱和Na2CO3溶液中,会导致溶液质量增加 | |
| D. | 金属Na失火,可用CO2灭火 |
17. (1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.
(1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.
(2)Bodensteins 研究了下列反应:2HI(g)?H2(g)+I2(g)在 716K 时,气体混合物中碘化氢的物质的量分数 x(HI)与反应时间 t 的关系如表:
①根据上述实验结果,该反应的平衡常数K的计算式为$\frac{0.10{8}^{2}}{0.78{4}^{2}}$.
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为$\frac{{K}_{正}}{K}$(以K和k正表示).若 k正=0.0027min-1,在 t=40min 时,v正=1.95×10-3 min-1.
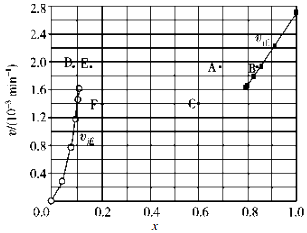
③由上述实验数据计算得到v正~x(HI)和 v逆~x(H2)的关系如图所示.当升高到某一温度时,反应重新达到平衡,相应的点依次为A(填字母)和E(填字母).
 (1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.
(1)已知反应 2HI(g)?H2(g)+I2(g)的△H=+11kJ/mol,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为299kJ.(2)Bodensteins 研究了下列反应:2HI(g)?H2(g)+I2(g)在 716K 时,气体混合物中碘化氢的物质的量分数 x(HI)与反应时间 t 的关系如表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为$\frac{{K}_{正}}{K}$(以K和k正表示).若 k正=0.0027min-1,在 t=40min 时,v正=1.95×10-3 min-1.
③由上述实验数据计算得到v正~x(HI)和 v逆~x(H2)的关系如图所示.当升高到某一温度时,反应重新达到平衡,相应的点依次为A(填字母)和E(填字母).