题目内容
18.几种短周期元素的原子半径及主要化合价如表:| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | R的氧化物对应的水化物可能具有两性 | |
| B. | L、M的单质与稀硫酸反应速率:M>L | |
| C. | T、Q的氢化物常态下均为无色气体 | |
| D. | L、Q形成的简单离子核外电子数相等 |
分析 在主族元素中,元素的最高化合价与其族序数相等,原子的电子层数越多其原子半径越大,根据元素化合价知,L、R属于第IIA元素,L的原子半径大于R,则L是Mg元素、R是Be元素;
M属于第IIIA族元素,M原子半径大于R,所以M是Al元素;
Q最高化合价是+6价,最低负价是-2价,则Q是S元素;
T元素最低负价是-2价,则T是O元素,再结合物质结构、性质解答.
解答 解:在主族元素中,元素的最高化合价与其族序数相等,原子的电子层数越多其原子半径越大,根据元素化合价知,L、R属于第IIA元素,L的原子半径大于R,则L是Mg元素、R是Be元素;M属于第IIIA族元素,M原子半径大于R,所以M是Al元素;Q最高化合价是+6价,最低负价是-2价,则Q是S元素;T元素最低负价是-2价,则T是O元素,
A.Al的氧化物对应的水化物Al(OH)3,能与强酸反应也能与强碱反应,具有两性,故A正确;
B.L是Mg元素、M为Al元素,金属越活泼,与酸反应速率越大,则单质与稀硫酸反应速率:L>M,故B错误;
C.Q为S元素,其的氢化物常态下为无色气体,T为O元素,水在常态下是液体,故C错误;
D.L是Mg元素,Q是S元素,L、Q形成的简单离子核外电子数分别为10、18,故D错误;
故选A.
点评 本题考查了原子结构和元素性质,明确元素化合价、原子半径与原子结构和元素族序数之间的关系即可解答,题目难度中等.

练习册系列答案
相关题目
6.2016年4月16日凌晨日本南部九州地区发生的7.3级地震,九州阿苏地区发生了大规模山体滑坡及火山爆发,其周边区域的空气中漂浮着放射性物质,其中含有碘的同位素13153I,13153I中的质子数为( )
| A. | 53 | B. | 78 | C. | 131 | D. | 184 |
3.下列化学用语表示正确的是( )
| A. | CO2的电子式为: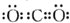 | |
| B. | S2-的离子离子结构示意图是: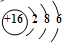 | |
| C. | 原子核内有18个中子的氯原子:3518Cl | |
| D. | HBr电子式为: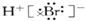 |
7.下列化学用语描述中不正确的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | K2O的电子式: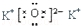 | |
| C. | 2-乙基-1,3-丁二烯分子的键线式: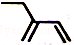 | |
| D. | 比例模型  可以表示CO2分子或SiO2 可以表示CO2分子或SiO2 |