题目内容
6.通过以下反应均可获取H2.下列有关说法正确的是( )①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
| A. | 反应CH4(g)═C(s)+2 H2(g)的△H4=+74.8kJ•mol-1 | |
| B. | 反应①中电能转化为化学能 | |
| C. | 反应②中反应物的总能量高于生成物的总能量 | |
| D. | 反应③使用催化剂,△H3减小 |
分析 A.由盖斯定律可知,③-②得到CH4(g)═C(s)+2 H2(g);
B.反应①中太阳能转化为化学能;
C.反应②中△H>0,为吸热反应;
D.催化剂可改变反应的途径,不改变始终态.
解答 解:A.由盖斯定律可知,③-②得到CH4(g)═C(s)+2 H2(g),则△H4=(+206.1kJ•mol-1)-(+131.3kJ•mol-1)=+74.8kJ•mol-1,故A正确;
B.反应①中太阳能转化为化学能,没有外加电源,故B错误;
C.反应②中△H>0,为吸热反应,则反应物的总能量低于生成物的总能量,故C错误;
D.催化剂可改变反应的途径,不改变始终态,则使用催化剂,△H3不变,故D错误;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、盖斯定律应用、能量转化为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
16.下列不能用于判断F 和 Cl的非金属性强弱的事实是( )
| A. | 气态氢化物的稳定性 | B. | 最高价氧化物对应的水化物的酸性 | ||
| C. | 单质与氢气反应的难易 | D. | F-和Cl-的还原性 |
17.胶体区别于其他分散系的根本原因是( )
| A. | 胶体粒子带电 | B. | 胶体粒子不可穿过半透膜 | ||
| C. | 分散质粒子直径在1~100 nm之间 | D. | 胶体有丁达尔现象 |
1.下列镁的化合物中,能与稀盐酸反应并生成无色有刺激性气味气体的是( )
| A. | MgO | B. | MgCO3 | C. | Mg2(OH)2CO3 | D. | Mg3N2 |
11.化学与环境密切相关,下列有关说法错误的是( )
| A. | NO2、NO含氮氧化物是光化学烟雾的主要污染物 | |
| B. | 酸性物质的排放加以控制,开发新清洁能源是减少酸雨的有效措施 | |
| C. | CO2、NO2或SO2都会导致酸雨的形成 | |
| D. | 大气中CO2含量的增加会导致温室效应加剧 |
15.200mL Fe2(SO4)3溶液中含Fe3+5.6g,溶液中SO42-的物质的量浓度是( )
| A. | 0.5mol/L | B. | 0.75 mol/L | C. | 1 mol/L | D. | 0.25 mol/L |
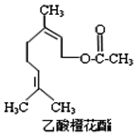 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )