题目内容
16.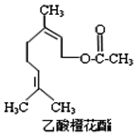 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( ) ①分子式为C12H20O2
②能使酸性KMnO4溶液褪色,但不能使溴水褪色
③能发生的反应类型有:加成、取代、氧化、加聚
④它的同分异构体中可能有芳香族化合物
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol.
| A. | ①②③ | B. | ①②⑤ | C. | ②④⑥ | D. | ②⑤⑥ |
分析 由结构可知分子式,分子中含碳碳双键、-COOC-,结合烯烃和酯的性质来解答.
解答 解:①由结构可知分子式为C12H20O2,故正确;
②含有碳碳双键,可发生氧化反应,能使酸性KMnO4溶液褪色,发生加成反应而能使溴水褪色,故错误;
③含有碳碳双键,可发生加成、加聚和氧化反应,含有酯基,可发生取代,故正确;
④有机物含有3个双键,对应同分异构体中不可能为芳香族化合物,因芳香族化合物的不饱和度至少为4,故错误;
⑤1mol该有机物水解生成1mol羧基,只能消耗1mol NaOH,故正确;
⑥只有碳碳双键能与氢气发生加成反应,1mol该有机物在一定条件下和H2反应,共消耗H2为2mol,故错误.
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握常见有机物的官能团为解答的关键,熟悉烯烃、酯的性质即可解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ•mol-1
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ•mol-1.
| A. | 反应CH4(g)═C(s)+2 H2(g)的△H4=+74.8kJ•mol-1 | |
| B. | 反应①中电能转化为化学能 | |
| C. | 反应②中反应物的总能量高于生成物的总能量 | |
| D. | 反应③使用催化剂,△H3减小 |
4.乙稀利(C2H6ClO3P)植物生长调节剂,它可由环氧乙烧和PCl3为原料合成.相关表示不正确的是( )
| A. | 环氧乙烷的结构简式:C2H4O | B. | 中子数为16的磷原子:${\;}_{15}^{16}$P | ||
| C. | 氯原子的结构示意图: | D. | PC13的电子式: |
11.以下数值大于或等于阿伏伽德罗常数的是( )
| A. | 常温常压下,5.6L甲烷中的共价键数目 | |
| B. | 标准状况下,17gND3中所含分子数目 | |
| C. | 向0.2 mol NH4Al(SO4)2溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目 | |
| D. | 0.1mol羟基(-OH)中所含电子数目 |
1.已知反应CaCO3 (s)+2HCl(aq)═CaCl2 (aq)+CO2(g)+H2O(l),下列措施可使产生CO2的速率加快的是( )
| A. | 加大CaCO3的量 | B. | 加大盐酸的浓度 | C. | 加大盐酸的量 | D. | 减少CaCl2的浓度 |
8.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 65gKHSO4晶体中含有SO42-的数目为0.5NA | |
| B. | 把含0.1molFeCl3的浓溶液加入沸水中形成0.1NA个氢氧化铁胶体 | |
| C. | 常温常压下,7.0g乙烯与丙烯的混合物中含有碳氢键的数目为NA | |
| D. | 50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
6.硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当SO42-的浓度为0.20mol•L-1时,加入等体积的0.20mol•L-1的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是( )
| A. | 0.20 mol•L-1 | B. | 0.25 mol•L-1 | C. | 0.225 mol•L-1 | D. | 0.45 mol•L-1 |