题目内容
有关电解质溶液下列说法正确的是
A.等体积、等浓度的Na2CO3、NaHCO3溶液混合后,3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
B.常温下pH=2的盐酸和pH=12的氨水等体积混合后c(Cl-)+c(H+)<c(NH4+)+c(OH-)
C.若一元酸酸性HA>HB,则等体积、等浓度的NaA与NaB溶液中,前者的离子总数小于后者
D.将AlCl3溶液、Na2SO3溶液蒸干并灼烧可以得到Al2O3、Na2SO3
练习册系列答案
相关题目
18.如表是实验室制备气体的有关内容:
(1)上述气体中从制备过程看,必须选择合适的氧化剂才能实现的是Cl2(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是SO2;
(2)根据表中所列实验原理,从如图1装置中选择合适的气体发生装置,将其编号填入上表中的空格中.

(3)某学习小组设计了如图2实验,将氯气依次通过下列装置以验证氯气的性质:
①通入氯气后,A中的现象是溶液变蓝色,整套实验装置存在的明显缺陷是无尾气吸收装置;
②C装置中发生反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-.
③该小组同学欲设计一个实验,证明洗气瓶B中的Na2SO3己被氧化.具体操作为:取一定量的B中溶液于一洁净的试管中,向其中加入硝酸酸化的硝酸钡溶液后,若产生白色沉淀则证明已经被氧化.你认为否 (填“是”或“否”)合理?
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | Ⅲ |
| ② | 制备二氧化硫 | Na2SO3→SO2 | Ⅲ |
| ③ | 制备氯气 | HCl→Cl2 | Ⅰ或Ⅲ |
(2)根据表中所列实验原理,从如图1装置中选择合适的气体发生装置,将其编号填入上表中的空格中.

(3)某学习小组设计了如图2实验,将氯气依次通过下列装置以验证氯气的性质:
①通入氯气后,A中的现象是溶液变蓝色,整套实验装置存在的明显缺陷是无尾气吸收装置;
②C装置中发生反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-.
③该小组同学欲设计一个实验,证明洗气瓶B中的Na2SO3己被氧化.具体操作为:取一定量的B中溶液于一洁净的试管中,向其中加入硝酸酸化的硝酸钡溶液后,若产生白色沉淀则证明已经被氧化.你认为否 (填“是”或“否”)合理?
19.以 NA表示阿伏加德罗常数的值,下列说法正确的是( )


| A. | 18g 冰(图甲)中含 O-H 键数目为 4NA | |
| B. | 28g 晶体硅(图乙)中含有σ键数目为 2NA | |
| C. | 44g 干冰(图丙)中含有 NA个晶胞结构单元 | |
| D. | 石墨烯(图丁)是碳原子单层片状新材料,12g 石墨烯中含π键数目为 1.5NA |
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 在相同温度下,pH=1且体积为1L的硫酸溶液所含的H+数与pH=13且体积为1L的氢氧化钠溶液所含的OH-数一定均为0.1NA | |
| B. | 7.8gNa2S和Na2O2的混合物中所含离子数为0.3NA | |
| C. | 在反应KClO4+8HCl=KCl+4Cl2↑+4H2O中,每生成4molCl2,转移的电子数为8NA | |
| D. | 在标准状况下,2.24LHF中含有的电子数为NA |
16.化学知识在生产和生活中有着重要的应用.下列说法中,正确的是( )
| A. | 与铜质水龙头连接处的钢质水管不易发生腐蚀 | |
| B. | 一种金属元素可能有多种氧化物,同一金属同一价态也可能有多种氧化物 | |
| C. | 金属钠、镁等金属着火时,可以使用泡沫灭火器来灭火 | |
| D. | 工业上可用铝热反应大规模炼铁 |


 SO3(g)的平衡常数K1=20,在同一温度下,反应2SO3(g)
SO3(g)的平衡常数K1=20,在同一温度下,反应2SO3(g) 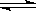 qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
qZ(g)△H>0,m+n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是