��Ŀ����
��Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ�Ϻϳɼ״��ķ�ӦΪ��CO��g��+2H2��g��?CH3OH��g������H
��1����֪���÷�Ӧ��300�棬5MPa���������Է����У����H 0����S 0 �����������=������
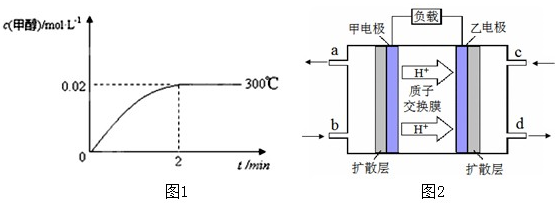
��2����300�棬5MPa�����£���0.20mol�� CO��0.58mol H2�Ļ���������2L�ܱ�����������Ӧ����Ӧ�����м״������ʵ���Ũ����ʱ��ı仯��ͼ1��ʾ��
����0��2min�ڣ���H2��ʾ��ƽ����Ӧ����Ϊ mol?L-1?s-1��
����ʽ����300��ʱ�÷�Ӧ��ƽ�ⳣ��K= ��
��300��ʱ����0.50mol CO��1.00mol H2��1.00mol CH3OH�����ݻ�Ϊ2L���ܱ������У���ʱ��Ӧ�� ��
A�����������ƶ� B�����淽���ƶ� C������ƽ��״̬ D�����ж�
�����д�ʩ�����Ӽ״����ʵ���
A��ѹ��������� B����CH3OH��g������ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���0.20mol CO��0.58mol H2
��3���״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ���ȼ�ϵ�صĵ�ط�ӦʽΪ��CH3OH��l��+
O2��g���TCO2��g��+2H2O��l�����乤��ԭ��ʾ��ͼ��ͼ2��
����ͼ�ĺ����ϱ��a��b��c��d�ĸ������ͨ����ų����������ƣ���ѧʽ�������ĵ缫��ӦʽΪ ��

��1����֪���÷�Ӧ��300�棬5MPa���������Է����У����H
��2����300�棬5MPa�����£���0.20mol�� CO��0.58mol H2�Ļ���������2L�ܱ�����������Ӧ����Ӧ�����м״������ʵ���Ũ����ʱ��ı仯��ͼ1��ʾ��
����0��2min�ڣ���H2��ʾ��ƽ����Ӧ����Ϊ
����ʽ����300��ʱ�÷�Ӧ��ƽ�ⳣ��K=
��300��ʱ����0.50mol CO��1.00mol H2��1.00mol CH3OH�����ݻ�Ϊ2L���ܱ������У���ʱ��Ӧ��
A�����������ƶ� B�����淽���ƶ� C������ƽ��״̬ D�����ж�
�����д�ʩ�����Ӽ״����ʵ���
A��ѹ��������� B����CH3OH��g������ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���0.20mol CO��0.58mol H2
��3���״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ���ȼ�ϵ�صĵ�ط�ӦʽΪ��CH3OH��l��+
| 3 |
| 2 |
����ͼ�ĺ����ϱ��a��b��c��d�ĸ������ͨ����ų����������ƣ���ѧʽ�������ĵ缫��ӦʽΪ
���㣺��Ӧ�Ⱥ��ʱ�,��ѧ��Դ���͵��,��ѧƽ�ⳣ���ĺ���,��ѧƽ���Ӱ������,��ѧƽ��ĵ�������
ר�⣺��ѧ��Ӧ�е������仯,��ѧƽ��ר��,�绯ѧר��
��������1������H-T��S��0ʱ����Ӧ�Է����У���Ϸ���ʽ�������ɣ�
��2���پ�ͼ��������c�͡�t���������
����������ʽ�����
�۾ݸ��¶��µ�K��Qc�Ƚϣ���K��Qcʱƽ�������ƶ���K��Qcʱƽ�������ƶ���
�ܽ��Ӱ��ƽ���ƶ������أ�ʹƽ�������ƶ����ɣ�
��3���״�-����ȼ�ϵ���Ǽ״���������Ӧ��������ԭ��Ӧ���״��ڷ�Ӧ��ʧȥ���ӷ���������Ӧ��ԭ���������������Ӧ���ɶ�����̼�������������ϵõ������������������ӣ��������ӽ�����������ˮ���缫��Ӧ���ݵ�ط�Ӧ�������缫��Ӧ����õ���
��2���پ�ͼ��������c�͡�t���������
����������ʽ�����
�۾ݸ��¶��µ�K��Qc�Ƚϣ���K��Qcʱƽ�������ƶ���K��Qcʱƽ�������ƶ���
�ܽ��Ӱ��ƽ���ƶ������أ�ʹƽ�������ƶ����ɣ�
��3���״�-����ȼ�ϵ���Ǽ״���������Ӧ��������ԭ��Ӧ���״��ڷ�Ӧ��ʧȥ���ӷ���������Ӧ��ԭ���������������Ӧ���ɶ�����̼�������������ϵõ������������������ӣ��������ӽ�����������ˮ���缫��Ӧ���ݵ�ط�Ӧ�������缫��Ӧ����õ���
���
�⣺��1���÷�Ӧ�ķ�Ӧ����3mol���壬��������1mol���壬���ԡ�S��0����Ӧ�Է����С�H-T��S��0���ʡ�H����С��0���ʴ�Ϊ����������
��2����2minʱ���״�Ũ�ȱ仯0.02mol/L��������Ũ�ȱ仯Ϊ0.04mol/L��v��H2��=
=
=0.02mol/��L?min��-1
�ʴ�Ϊ��0.02��
��CO��g��+2H2��g��?CH3OH��g��
����ģ�mol/L�� 0.10 0.29 0
��Ӧ�ģ�mol/L�� 0.02 0.04 0.02
ƽ���mol/L�� 0.08 0.25 0.02
K=
=
��mol/L��-2=4��mol/L��-2
�ʴ�Ϊ��K=4��mol/L��-2��
��Qc=K=
=
=8��K=4������ƽ�������ƶ���ѡB��
�ʴ�Ϊ��B��
��A�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g������Ӧ������������������ѹ���������ʱ��ѹǿ����ƽ�������ƶ��������Ӽ״����ʣ�A��ȷ��
B��������״���ƽ�������ƶ������Ӽ״����ʣ���B��ȷ��
C������He����Ӱ�������ķ�ѹ��ƽ�ⲻ�ƶ����������Ӽ״����ʣ���C����
D��������䣬�ٳ��뷴Ӧ�����壬ƽ�������ƶ��������Ӽ״����ʣ���D��ȷ��
��ѡ��ABD��
��3���ټ״�-����ȼ�ϵ���Ǽ״���������Ӧ��������ԭ��Ӧ���״��ڷ�Ӧ��ʧȥ���ӷ���������Ӧ��ԭ���������������Ӧ���ɶ�����̼�������������ϵõ������������������ӣ��������ӽ�����������ˮ������a�ų�CO2��bͨ��״�ˮ��Һ��cͨ��O2��d����ˮ����ע��ͼ��
 ��
��
��ط�ӦΪ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l����
���������ӦΪ��O2+4H++4e-=2H2O��
��ط�Ӧ-������Ӧ��3�õ������缫��ӦΪ��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
�ʴ�Ϊ�� ��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
��2����2minʱ���״�Ũ�ȱ仯0.02mol/L��������Ũ�ȱ仯Ϊ0.04mol/L��v��H2��=
| ��c |
| ��t |
| 0.04mol/L |
| 2min |
�ʴ�Ϊ��0.02��
��CO��g��+2H2��g��?CH3OH��g��
����ģ�mol/L�� 0.10 0.29 0
��Ӧ�ģ�mol/L�� 0.02 0.04 0.02
ƽ���mol/L�� 0.08 0.25 0.02
K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.02 |
| 0.08��0.252 |
�ʴ�Ϊ��K=4��mol/L��-2��
��Qc=K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.50 |
| 0.25��0.502 |
�ʴ�Ϊ��B��
��A�����ڷ�ӦCO��g��+2H2��g��?CH3OH��g������Ӧ������������������ѹ���������ʱ��ѹǿ����ƽ�������ƶ��������Ӽ״����ʣ�A��ȷ��
B��������״���ƽ�������ƶ������Ӽ״����ʣ���B��ȷ��
C������He����Ӱ�������ķ�ѹ��ƽ�ⲻ�ƶ����������Ӽ״����ʣ���C����
D��������䣬�ٳ��뷴Ӧ�����壬ƽ�������ƶ��������Ӽ״����ʣ���D��ȷ��
��ѡ��ABD��
��3���ټ״�-����ȼ�ϵ���Ǽ״���������Ӧ��������ԭ��Ӧ���״��ڷ�Ӧ��ʧȥ���ӷ���������Ӧ��ԭ���������������Ӧ���ɶ�����̼�������������ϵõ������������������ӣ��������ӽ�����������ˮ������a�ų�CO2��bͨ��״�ˮ��Һ��cͨ��O2��d����ˮ����ע��ͼ��
 ��
����ط�ӦΪ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l����
���������ӦΪ��O2+4H++4e-=2H2O��
��ط�Ӧ-������Ӧ��3�õ������缫��ӦΪ��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
�ʴ�Ϊ��
 ��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
��CH3OH��l��+H2O��l��-6e-=CO2��g��+6H+��
���������⿼���˻�ѧ��Ӧ�ķ�Ӧ�ȵļ��㡢ԭ��صIJ����жϺ͵缫�жϣ��缫��Ӧ����˹���ɵļ���Ӧ�ã���������ǹؼ���ԭ���ԭ���dz����ص㣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
��̼����������ָͨ��һ���ķ�������ҵ�����в�����CO2������������ã��������NaOH��Һ��������CO2���������������ͼ��ʾ����������������δ������������йظ÷����������в���ȷ���ǣ�������
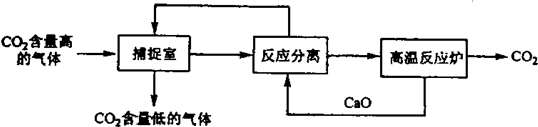

| A���ܺĴ��Ǹ÷�����һ��ȱ�� |
| B�����������У�����������ԭ��Ӧ���з�������ԭ��Ӧ |
| C������Ӧ���롱�����У�����Ļ��������ǹ��� |
| D�����������У���2�����ʿ���ѭ������ |
���ʵ���Ũ����ȵİ�ˮ��Һ��������Һ�������ϣ����йػ����Һ������Ũ�ȹ�ϵ����ȷ���ǣ�������
| A��c��SO42-����c��H+����c��NH4+����c��OH-�� |
| B��c��H+����c��SO42-����c��NH4+����c��OH-�� |
| C��c��OH-��-c��NH4+��=c��H+��-2c��SO42-�� |
| D��c��OH-��+c��NH3?H2O��=c��H+��-c��SO42-�� |