题目内容
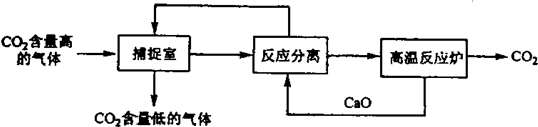
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出).下列有关该方法的叙述中不正确的是( )

| A、能耗大是该方法的一大缺点 |
| B、整个过程中,既有氧化还原反应又有非氧化还原反应 |
| C、“反应分离”环节中,分离的基本操作是过滤 |
| D、整个过程中,有2种物质可以循环利用 |
考点:碳族元素简介,氧化还原反应
专题:信息给予题
分析:根据题中信息可知,基本过程中有两个反应:①二氧化碳与氢氧化钠反应,②碳酸钙的高温分解,循环利用的应该有CaO和NaOH两种物质,捕捉室中反应为二氧化碳与氢氧化钠反应,得到的Na2CO3和CaO在溶液中反应得到NaOH和CaCO3,以此解答.
解答:
解:A.碳酸钙的分解在高温条件下进行,消耗大量能量,是该方法的一大缺点,故A正确;
B.基本过程中有两个反应:①二氧化碳与氢氧化钠反应,②碳酸钙的高温分解,都属于非氧化还原反应,故B错误;
C.“反应分离”过程中分离物质的操作应该是过滤,目的是通过过滤得到碳酸钙沉淀,故C正确;
D.循环利用的有CaO和NaOH两种物质,故D正确;
故选B.
B.基本过程中有两个反应:①二氧化碳与氢氧化钠反应,②碳酸钙的高温分解,都属于非氧化还原反应,故B错误;
C.“反应分离”过程中分离物质的操作应该是过滤,目的是通过过滤得到碳酸钙沉淀,故C正确;
D.循环利用的有CaO和NaOH两种物质,故D正确;
故选B.
点评:本题考查了物质分离和提纯的实验方案设计,明确各个流程中发生的反应是解本题关键,注意从整体上把握,难度不大.

练习册系列答案
 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
 镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )
镁燃料电池具有比能量高、安全方便、成本低等特点,常用的有镁-次氯酸盐燃料电池,镁-过氧化氢燃料电池等,图为镁-次氯酸盐燃料电池的工作原理图,下列说法不正确的是( )| A、电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl- |
| B、放电过程中OH-移向正极 |
| C、镁电池中镁均为负极,发生氧化反应 |
| D、镁-过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O |
下列反应属于吸热反应的是( )
| A、氢氧化钠与硝酸反应 |
| B、铁与盐酸反应 |
| C、氢氧化钡与氯化铵反应 |
| D、氧化钙与水反应 |
下列离子方程式书写正确的是( )
| A、澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-→CaCO3↓+H2O |
| B、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
| C、向NaHSO4溶液中滴加Ba(OH)2至刚好沉淀完全:H++SO42-+Ba2++OH-→BaSO4↓+H2O |
| D、向含有0.1 mol溶质的FeI2溶液中通入0.1 mol的Cl2:2Fe+2I-+2Cl2→2Fe3++I2+4Cl- |
 是由一种单体缩聚而成的,该单体的键线式为
是由一种单体缩聚而成的,该单体的键线式为 )滴入Na2CO3溶液中发生的化学方程式:
)滴入Na2CO3溶液中发生的化学方程式:
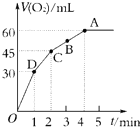 加入0.1mol MnO2粉末于50mL过氧化氢溶液(H2O2,ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
加入0.1mol MnO2粉末于50mL过氧化氢溶液(H2O2,ρ=1.1g?mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.