题目内容
3.下列说法错误的是( )| A. | 非金属两原子间不可能形成离子键 | |
| B. | 非金属元素不可能形成离子化合物 | |
| C. | 含有非极性键的分子,不一定是共价化合物 | |
| D. | 离子化合物中一定不含共价键 |
分析 A.非金属元素之间易形成共价键;
B.非金属元素可能形成离子键化合物;
D.含有非极性键的分子,可能是单质;
D.离子化合物中可能含有共价键.
解答 解:A.非金属元素之间易形成共价键,所以非金属两原子间不可能形成离子键,故A正确;
B.非金属元素可能形成离子键化合物,如铵盐,故B错误;
D.含有非极性键的分子,可能是单质,如氮气、氢气等,故C正确;
D.离子化合物中可能含有共价键,如KOH等,故D错误;
故选BD.
点评 本题考查化学键与化合物的关系,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,注意采用举例法分析解答,题目难度不大.

练习册系列答案
相关题目
13.下列各组粒子中粒子半径由小到大的是( )
| A. | O2- Na+Mg2+Al3+ | B. | O P S Cl | ||
| C. | A l3+Mg2+ Na+ F- | D. | K+ Mg2+ Al3+ H+ |
14.关于丙烯醛(CH2=CH-CHO)的下列叙述中,不正确的是( )
| A. | 在丙烯醛分子中,含有两种官能团 | |
| B. | 丙烯醛能发生加聚反应,生成高聚物  | |
| C. | 等物质的量的丙烯醛和丙醛完全燃烧,消耗等物质的量的O2 | |
| D. | 丙烯醛能使溴水褪色,能使酸性高锰酸钾溶液褪色 |
8.下列化学用语使用正确的是( )
| A. | NH4Cl的电子式: | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 氧化钠的电子式: | |
| D. | R2+离子核外有a个电子,b个中子,R原子表示为:${\;}_{a+2}^{a+b+2}$R |
15.X、Y、Z、W为四种短周期主族元素,原子序数依次增大.其中X、Z同主族,Y、Z同周期,Y原子的最外层电子数是次外层电子数的一半,X原子最外层电子数是核外电子层数的3倍,W的最高正价与最低负价代数和为6.下列说法正确的是( )
| A. | X、Y、Z、W四种元素的简单氢化物中,Y的气态氢化物最稳定 | |
| B. | Y、Z、W四种元素的原子半径由大到小的顺序为:Y>Z>W | |
| C. | X、Z和W三种元素形成的简单离子的半径由大到小的顺序为:W>Z>X | |
| D. | Y、Z和W三种元素的最高价氧化物对应的水化物都是强酸 |
12.锌锰干电池是家庭常用的电池,该电池工作时发生的化学反应为Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+2MnO(OH),下列说法正确的是( )
| A. | 电池工作时锌片作为正极 | |
| B. | 电池工作时从负极向外电路输出电子 | |
| C. | 电池工作时MnO2发生还原反应 | |
| D. | 电池工作时电能向化学能转化 |
13.雾霾天气是一种大气污染状态,其污染的来源多种多样,如汽车尾气、工业排放、建筑扬尘、垃圾焚烧等.
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化.
①已知部分化学键的键能如下
请完成汽车尾气净化中发生反应的热化学方程式
2NO(g)+2CO(g)?N2(g)+2CO2(g) Q=-538KJ
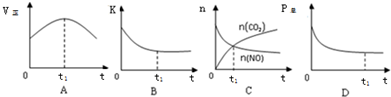
②若上述反应在恒温、恒容的密闭体系中进行,t1时刻达到平衡状态,则下列示意图不符合题意的是ABC(填选项序号).
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.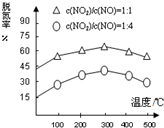
在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答:温度对脱氮率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小.
NH4Al (SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(3)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水.(用必要的方程式说明);相同条件下,0.1mol•L-1 NH4HSO4中c(NH4+)>(填“=”、“>”或“<”)0.1mol•L-1NH4Al(SO4)2中c(NH4+).

(4)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图象.①其中符合0.1mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是A(填写字母);
(5)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化.
①已知部分化学键的键能如下
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
2NO(g)+2CO(g)?N2(g)+2CO2(g) Q=-538KJ
②若上述反应在恒温、恒容的密闭体系中进行,t1时刻达到平衡状态,则下列示意图不符合题意的是ABC(填选项序号).

(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.

在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答:温度对脱氮率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小.
NH4Al (SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(3)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水.(用必要的方程式说明);相同条件下,0.1mol•L-1 NH4HSO4中c(NH4+)>(填“=”、“>”或“<”)0.1mol•L-1NH4Al(SO4)2中c(NH4+).

(4)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图象.①其中符合0.1mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是A(填写字母);
(5)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).






 .
.