题目内容
12.锌锰干电池是家庭常用的电池,该电池工作时发生的化学反应为Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+2MnO(OH),下列说法正确的是( )| A. | 电池工作时锌片作为正极 | |
| B. | 电池工作时从负极向外电路输出电子 | |
| C. | 电池工作时MnO2发生还原反应 | |
| D. | 电池工作时电能向化学能转化 |
分析 A、原电池中负极上发生失电子的氧化反应;
B、电池中电子从负极流向正极;
C、化合价升高元素发生氧化反应,化合价降低元素发生还原反应;
D、电池是将化学能转化为电能的装置.
解答 解:A、根据电池反应:Zn+2NH4C1+2Mn02═Zn( NH3)2C12+2MnO(OH),原电池中负极上是金属锌发生失电子的氧化反应,故A错误;
B、电池中电子从负极流向正极,故B错误;
C、电池工作时,Mn02中Mn的化合价降低,发生还原反应,故C正确;
D、电池是将化学能转化为电能的装置,故D错误.
故选C.
点评 本题考查了原电池原理,根据得失电子判断正负极及其反应,再结合离子移动方向、盐类水解来分析解答,难度不大.

练习册系列答案
相关题目
3.下列说法错误的是( )
| A. | 非金属两原子间不可能形成离子键 | |
| B. | 非金属元素不可能形成离子化合物 | |
| C. | 含有非极性键的分子,不一定是共价化合物 | |
| D. | 离子化合物中一定不含共价键 |
20.下列说法中,正确的是( )
| A. | 乙醛分子中的所有原子都在同一平面上 | |
| B. | 凡是能发生银镜反应的有机物都是醛 | |
| C. | 完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等 | |
| D. | 醛类既能被氧化为羧酸,又能被还原为醇 |
4.下列灭火剂能用于扑灭金属钠着火的是( )
| A. | 干冰灭火剂 | B. | 沙土 | C. | 干粉灭火剂 | D. | 泡沫灭火剂 |
1.碱性锌锰电池是最常见的一次电池,它的总反应如下:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH由此可知,该电池放电时的负极材料是( )
| A. | Zn | B. | Zn(OH)2 | C. | MnO2 | D. | MnOOH |
5.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.
已知:C3H8(g)═CH4(g)+C2H2(g)+H2(g)△H1=+156.6kJ•mol-1
C3H6 (g)═CH4(g)+C2H2(g)△H2=+32.4kJ•mol-1
则相同条件下,反应C3H8(g)═C3H6 (g)+H2(g) 的△H 正确是( )
已知:C3H8(g)═CH4(g)+C2H2(g)+H2(g)△H1=+156.6kJ•mol-1
C3H6 (g)═CH4(g)+C2H2(g)△H2=+32.4kJ•mol-1
则相同条件下,反应C3H8(g)═C3H6 (g)+H2(g) 的△H 正确是( )
| A. | △H=一124.2kJ•mol-1 | B. | △H=+124.2kJ•mol-1 | ||
| C. | △H=+248.4kJ•mol-1 | D. | 不能确定 |
 .
. .
.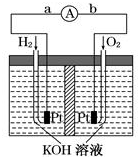 氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: