题目内容
11.写出下列物质的电子式:N2

H2S

H2O2

CO2

NaOH

NH4Cl

MgBr2
 .
.
分析 氮气中存在3对共用电子对,氮原子最外层达到8个电子;
H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H-S键;
双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
CO2为共价化合物,C原子和O原子间为双键;
氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
氯化铵为离子化合物,复杂阳离子和阴离子均需要括号;
溴化镁为离子化合物,溴离子和镁离子之间为离子键.
解答 解:氮气中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为 ;
;
H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H-S键,电子式为: ,
,
双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ;
;
CO2为共价化合物,C原子和O原子间为双键,故电子式为 ;
;
氢氧化钠属于离子化合物,电子式中需要标出阴阳离子所带电荷,钠离子直接用离子符号表示,氢氧根离子需要标出最外层电子,氢氧化钠的电子式为: ;
;
氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ;
;
溴化镁为离子化合物,溴离子和镁离子之间为离子键,故电子式为: .
.
故答案为: ;
; ;
; ;
; ;
; ;
; ;
; .
.
点评 本题考查了电子式的书写,题目难度中等,注意掌握电子式的概念及表示方法,明确离子化合物与共价化合物的电子式的表示方法及区别.

练习册系列答案
相关题目
1.在下列物质中,分别加入金属钠,不能产生氢气的是( )
| A. | 水 | B. | 甲苯 | C. | 无水乙醇 | D. | 75%的酒精 |
19.下列除去括号内杂质的有关操作方法正确的是( )
| A. | 乙烷(乙炔):通过盛酸性高锰酸钾溶液的洗气瓶 | |
| B. | 乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热 | |
| C. | 苯(苯酚):加入NaCl溶液,然后分液 | |
| D. | 乙醇(水):加入生石灰,然后蒸馏 |
16.分子式为C9H11Cl,且苯环上有两个取代基的芳香族化合物,其可能的结构有(不考虑立体异构)( )
| A. | 5种 | B. | 9种 | C. | 12种 | D. | 15种 |
3.下列说法错误的是( )
| A. | 非金属两原子间不可能形成离子键 | |
| B. | 非金属元素不可能形成离子化合物 | |
| C. | 含有非极性键的分子,不一定是共价化合物 | |
| D. | 离子化合物中一定不含共价键 |
20.下列说法中,正确的是( )
| A. | 乙醛分子中的所有原子都在同一平面上 | |
| B. | 凡是能发生银镜反应的有机物都是醛 | |
| C. | 完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等 | |
| D. | 醛类既能被氧化为羧酸,又能被还原为醇 |
1.碱性锌锰电池是最常见的一次电池,它的总反应如下:Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH由此可知,该电池放电时的负极材料是( )
| A. | Zn | B. | Zn(OH)2 | C. | MnO2 | D. | MnOOH |
 .
.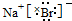 .
.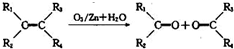 (其中R、R1、R2、R3和R4均表示烃基)
(其中R、R1、R2、R3和R4均表示烃基)