题目内容
18.某元素原子的最外层电子数与次外层电子数相同,且最外层电子数与次外层电子数之和小于8,它是( )| A. | 锂 | B. | 铍 | C. | 氦 | D. | 钙 |
分析 如果2个电子层,则是第一层2个电子,第二层也是2个电子,且符合最外层电子数与次外层电子数之和小于8,如果3个电子层,次外层即是第2层是8个电子,最外层也是8个电子,不符合最外层电子数与次外层电子数之和小于8,由此分析解答.
解答 解:如果2个电子层,则是第一层2个电子,第二层也是2个电子,且符合最外层电子数与次外层电子数之和小于8,如果3个电子层,次外层即是第2层是8个电子,最外层也是8个电子,不符合最外层电子数与次外层电子数之和小于8,所以是4号铍,
故选B.
点评 本题是对原子核外电子排布知识的考查,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
8.将下列溶液置于敞口容器中,溶液质量会出现增重的是( )
| A. | 浓氨水 | B. | 浓盐酸 | C. | 浓H2SO4 | D. | 浓硝酸 |
9.钡在氧气中燃烧时的得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是( ) 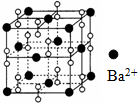

| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该晶体晶胞结构与CsCl相似 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有12个 |
13.表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
3.下列说法错误的是( )
| A. | 非金属两原子间不可能形成离子键 | |
| B. | 非金属元素不可能形成离子化合物 | |
| C. | 含有非极性键的分子,不一定是共价化合物 | |
| D. | 离子化合物中一定不含共价键 |
10.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>d | B. | 氢化物的稳定性:H2Y>HZ | ||
| C. | 离子的氧化性:X+<W3+ | D. | 原子半径:X<W |
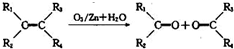 (其中R、R1、R2、R3和R4均表示烃基)
(其中R、R1、R2、R3和R4均表示烃基)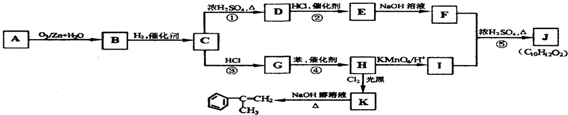
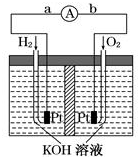 氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: