题目内容
室温下,下列溶液中粒子的物质的量浓度关系正确的是( )
| A、O.lmol/L NaHS溶液:c(H+)+c(Na+)=c(S2-)+c(HS-)+c(0H-) |
| B、O.lmol/L Na2C03溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.lmol/L |
| C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、浓度均为0.1 mol/L的①NH4Cl②NH4Al(SO4)2③NH4HCO3三种溶液,其中c(NH4+):③>①>② |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A、根据电荷守恒可知,c(H+)+c(Na+)=2c(S2-)+c(HS-)+c(0H-);
B、根据物料守恒,碳元素在溶液中所有存在形式的浓度之和为O.lmol/L;
C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合溶液呈酸性;
D、②NH4Al(S04)2电离产生的铝离子对铵根离子的水解起抑制作用,而③NH4HC03电离出的碳酸氢根离子对铵根离子的水解起促进作用.
B、根据物料守恒,碳元素在溶液中所有存在形式的浓度之和为O.lmol/L;
C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合溶液呈酸性;
D、②NH4Al(S04)2电离产生的铝离子对铵根离子的水解起抑制作用,而③NH4HC03电离出的碳酸氢根离子对铵根离子的水解起促进作用.
解答:
解:A、根据电荷守恒可知,c(H+)+c(Na+)=2c(S2-)+c(HS-)+c(0H-),故A错误;
B、根据物料守恒,碳元素在溶液中所有存在形式的浓度之和为O.lmol/L,所以c(H2C03)+c(HC03-)+c(C032-)=O.lmol/L,故B正确;
C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合溶液呈酸性,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D、②NH4Al(S04)2电离产生的铝离子对铵根离子的水解起抑制作用,而③NH4HC03电离出的碳酸氢根离子对铵根离子的水解起促进作用,所以其中c(NH4+):③<①<②,故D错误;
故选B.
B、根据物料守恒,碳元素在溶液中所有存在形式的浓度之和为O.lmol/L,所以c(H2C03)+c(HC03-)+c(C032-)=O.lmol/L,故B正确;
C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合溶液呈酸性,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D、②NH4Al(S04)2电离产生的铝离子对铵根离子的水解起抑制作用,而③NH4HC03电离出的碳酸氢根离子对铵根离子的水解起促进作用,所以其中c(NH4+):③<①<②,故D错误;
故选B.
点评:本题考查离子浓度大小的比较,难度较大,熟悉盐的水解和物料守恒、电荷守恒的相关知识,水解与电离的程度及相互影响是解答本题的关键.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
常温下在20mL 0.l mol?L-1 Na2A溶液(pH=11)中逐滴加入0.1mol/L的盐酸,溶液的pH逐渐降低,下列说法一定正确的是(NA表示阿伏加德罗常数)( )
| A、当盐酸加入10mL时,溶液中c(Na+)=2 c(HA-)+2c(A2-)+2 c(H2A) |
| B、当盐酸加入20mL时,溶液中c(Na+)>c(Cl-)>c(HA-)>c(H+)>c(OH-) |
| C、当盐酸加入20mL时,溶液中HA-的数目小于0.002NA |
| D、当盐酸加入40mL时,溶液中c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)+c(Cl-) |
下列各溶液中氯离子(Cl-)的物质的量浓度最大的是( )
| A、200 mL,0.5mol?L-1的NaCl溶液 |
| B、100 mL,0.5mol?L-1的MgCl2溶液 |
| C、150 mL,1mol?L-1的NaCl溶液 |
| D、50 mL,0.5mol?L-1的AlCl3溶液 |
下列各组中的两物质相互反应时,与反应条件和用量无关的是( )
| A、Na和O2 |
| B、Fe和FeCl3 |
| C、CO2和NaOH |
| D、AlCl3和NaOH |
已知HA为酸性略强于醋酸的一元弱酸,则在0.1mol?L-1 NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)+c(H+)=c(A-)+c(OH-) |
| C、c(Na+)+c(OH-)=c(A-)+c(H+) |
| D、c(Na+)>c(OH-)>c(A-)>c(H+) |
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),下列说法错误的是( )
| A、MnS的Ksp比CuS的Ksp大 | ||||
B、该反应达到平衡时:
| ||||
| C、往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大 | ||||
| D、MnS(s)的浊液中加入少量可溶性MnSO4固体后,c(S2-)变大 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X与W同主族,X、W的单质在标准状况下的状态不同.Y是空气中含量最高的元素,Z原子最外层电子数是其内层电子总数的3倍,Z2-与W+具有相同的电子层结构.下列说法正确的是( )
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、元素Y的简单气态氢化物的热稳定性比Z的强 |
| C、由X、Y、Z三种元素形成的化合物的水溶液可能呈碱性 |
| D、化合物X2Z2与W2Z2所含化学键类型完全相同 |
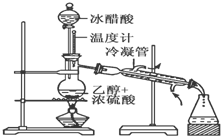 实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)