题目内容
下列各溶液中氯离子(Cl-)的物质的量浓度最大的是( )
| A、200 mL,0.5mol?L-1的NaCl溶液 |
| B、100 mL,0.5mol?L-1的MgCl2溶液 |
| C、150 mL,1mol?L-1的NaCl溶液 |
| D、50 mL,0.5mol?L-1的AlCl3溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:利用物质的构成及溶质的物质的量浓度来计算氯离子的浓度,与溶液的体积无关,溶液中C(Cl-)=溶质的物质的量浓度×化学式中氯离子个数,以此来解答.
解答:
解:A、200ml 0.5mol/L的NaCl溶液中Cl-离子的物质的量浓度为0.5mol/L×=0.5mol/L;
B、100mL 0.5mol/L的MgCl2溶液中Cl-离子的物质的量浓度为0.5mol/L×2=1mol/L;
C、150mL 1mol/L的NaCl溶液中Cl-离子的物质的量浓度为1mol/L×1=1mol/L;
D、50m L0.5mol/LAlCl3溶液中Cl-离子的物质的量浓度为0.5mol/L×3=1.5mol/L,
显然D中Cl-离子的物质的量浓度最大;
故选D.
B、100mL 0.5mol/L的MgCl2溶液中Cl-离子的物质的量浓度为0.5mol/L×2=1mol/L;
C、150mL 1mol/L的NaCl溶液中Cl-离子的物质的量浓度为1mol/L×1=1mol/L;
D、50m L0.5mol/LAlCl3溶液中Cl-离子的物质的量浓度为0.5mol/L×3=1.5mol/L,
显然D中Cl-离子的物质的量浓度最大;
故选D.
点评:本题考查物质的量浓度的有关计算,明确离子浓度与溶质的物质的量浓度的关系即可解答,较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
| A、若体积减小一半,则压强为原来的两倍 |
| B、平衡向右移动,混合气体颜色一定会变浅 |
| C、若体积减小一半,压强增大,但小于原来的两倍 |
| D、平衡向右移动,混合气体密度减小 |
室温下,下列溶液中粒子的物质的量浓度关系正确的是( )
| A、O.lmol/L NaHS溶液:c(H+)+c(Na+)=c(S2-)+c(HS-)+c(0H-) |
| B、O.lmol/L Na2C03溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.lmol/L |
| C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、浓度均为0.1 mol/L的①NH4Cl②NH4Al(SO4)2③NH4HCO3三种溶液,其中c(NH4+):③>①>② |
实验室里不同化学试剂的保存方法不尽相同,①NaOH溶液 ②大理石 ③NaCl溶液 ④稀硝酸4种试剂通常各自存放在如下图所示的玻璃试剂瓶中.按照试剂瓶的顺序存放试剂序号正确的是( )


| A、①②③④ | B、②①④③ |
| C、②③④① | D、②①③④ |
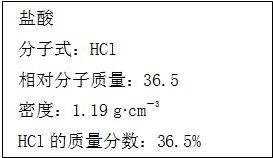 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: 如图进行实验,试管中现象对应的离子方程式不正确的是( )
如图进行实验,试管中现象对应的离子方程式不正确的是( )