题目内容
下列各组中的两物质相互反应时,与反应条件和用量无关的是( )
| A、Na和O2 |
| B、Fe和FeCl3 |
| C、CO2和NaOH |
| D、AlCl3和NaOH |
考点:钠的化学性质,镁、铝的重要化合物,铁的氧化物和氢氧化物
专题:几种重要的金属及其化合物
分析:A.钠和氧气反应生成氧化钠,钠在空气中燃烧生成过氧化钠;
B.无论FeCl3溶液是否过量,铁和FeCl3溶液反应都生成氯化亚铁;
C.少量氢氧化钠和二氧化碳反应生成碳酸氢钠,过量氢氧化钠和二氧化碳反应生成碳酸钠;
D.氯化铝和少量氢氧化钠反应生成氢氧化铝沉淀,和过量氢氧化钠反应生成偏铝酸钠.
B.无论FeCl3溶液是否过量,铁和FeCl3溶液反应都生成氯化亚铁;
C.少量氢氧化钠和二氧化碳反应生成碳酸氢钠,过量氢氧化钠和二氧化碳反应生成碳酸钠;
D.氯化铝和少量氢氧化钠反应生成氢氧化铝沉淀,和过量氢氧化钠反应生成偏铝酸钠.
解答:
解:A.Na和O2在不加热时生成Na2O,加热时生成Na2O2,反应条件不同,生成物不同,故A错误;
B.无论FeCl3溶液是否过量,铁和FeCl3溶液反应都生成氯化亚铁,故B正确;
C.NaOH和CO2少量反应生成Na2CO3,过量CO2反应生成NaHCO3,量不同,生成物不同,故C错误;
D.少量氢氧化钠和氯化铝反应AlCl3+4NaOH═NaAlO2+3NaCl+2H2O,过量氢氧化钠和氯化铝反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,反应物用量不同,产物不同,故D错误;
故选B.
B.无论FeCl3溶液是否过量,铁和FeCl3溶液反应都生成氯化亚铁,故B正确;
C.NaOH和CO2少量反应生成Na2CO3,过量CO2反应生成NaHCO3,量不同,生成物不同,故C错误;
D.少量氢氧化钠和氯化铝反应AlCl3+4NaOH═NaAlO2+3NaCl+2H2O,过量氢氧化钠和氯化铝反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,反应物用量不同,产物不同,故D错误;
故选B.
点评:本题考查了物质间的反应,明确物质的性质是解本题关键,反应物相同,如果反应条件不同、反应物浓度不同、反应物用量不同都会导致产物不同,题目难度不大.

练习册系列答案
相关题目
化学与人类生活、社会可持续发展密切相关.下列说法正确的是( )
| A、漂白粉的有效成分是Ca(ClO)2和CaCl2 |
| B、为消除碘缺乏病,我国政府规定在生产食用盐时必须加入一定量的单质碘 |
| C、向豆浆中加入盐卤可以做豆腐 |
| D、SO2的大量排放带来的环境问题是光化学烟雾和酸雨 |
室温下,下列溶液中粒子的物质的量浓度关系正确的是( )
| A、O.lmol/L NaHS溶液:c(H+)+c(Na+)=c(S2-)+c(HS-)+c(0H-) |
| B、O.lmol/L Na2C03溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.lmol/L |
| C、pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、浓度均为0.1 mol/L的①NH4Cl②NH4Al(SO4)2③NH4HCO3三种溶液,其中c(NH4+):③>①>② |
 如图进行实验,试管中现象对应的离子方程式不正确的是( )
如图进行实验,试管中现象对应的离子方程式不正确的是( )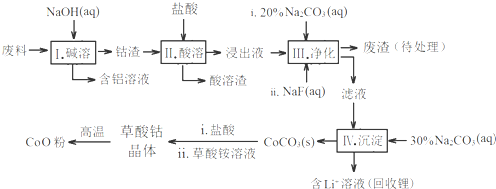
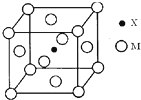 元素X基态原子的p电子比s电子少1个.元素Y基态原子的2p电子是2s电子的2倍.元素Z的一种单质为自然界硬度最大的物质.元素M位于第四周期,其基态原子失去3个电子后3d轨道半满.
元素X基态原子的p电子比s电子少1个.元素Y基态原子的2p电子是2s电子的2倍.元素Z的一种单质为自然界硬度最大的物质.元素M位于第四周期,其基态原子失去3个电子后3d轨道半满.