题目内容
一定条件下,在密闭容器中进行如下可逆反应:S2Cl2(l,橙黄色)+Cl2(g)?2SCl2(l,鲜红色)△H=-51.16kJ?mol-1.下列叙述中一定能表示该反应达到化学平衡状态的是( )
| A、单位时间内生成n mol S2Cl2,同时生成n mol Cl2(g) |
| B、单位时间内生成n mol Cl2,同时生成n mol SCl2(g) |
| C、混合物的颜色不再变化 |
| D、容器中S2Cl2、Cl2、SCl2的物质的量之比为1:1:2 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:看反应是否处于平衡状态,注意分析两个方面,一是正逆反应速率是否相等,二是各组分浓度是否变化,据此解答.
解答:
A、生成S2Cl2和生成Cl2(g)都是反应逆向进行,不能考查正逆反应速率相等,故A错误;
B、v逆(Cl2):v正(SCl2)=1:2时,正逆反应速率相等,故B错误;
C、混合气体的颜色不变,说明有色物质的浓度不变,各物质浓度不变,反应是平衡状态,故C正确;
D、各组分浓度不变,物质的量不变,但不一定是1:1:2,与加入物质的多少及转化率有关,故D错误.
故选:C.
B、v逆(Cl2):v正(SCl2)=1:2时,正逆反应速率相等,故B错误;
C、混合气体的颜色不变,说明有色物质的浓度不变,各物质浓度不变,反应是平衡状态,故C正确;
D、各组分浓度不变,物质的量不变,但不一定是1:1:2,与加入物质的多少及转化率有关,故D错误.
故选:C.
点评:考查化学平衡状态的判断,影响平衡移动的因素等,难度不大,注意理解平衡移动原理.

练习册系列答案
相关题目
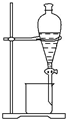
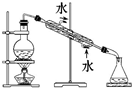
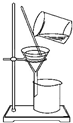
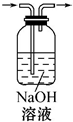
完成下列实验所需选择的装置或仪器都正确的是( )
| A | B | C | D | |
| 实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的氯化钾晶体 | 分离CCl4中的Br2 | 除去CO2气体中的HCl气体 |
| 装置 或仪器 |
 |
 |
 |
 |
| A、A | B、B | C、C | D、D |
下列关于元素周期律的叙述正确的是( )
| A、随着原子序数的递增,原子最外层电子数总是从1到8重复出现 |
| B、同主族元素的原子半径从上到下逐渐增大 |
| C、随着原子序数的递增,元素的最高正价从+1至+7,负价从-7至-1重复出现 |
| D、元素性质周期性变化是由原子半径周期性变化导致的 |
下列离子方程式中正确的是( )
| A、铜与稀硝酸反应:Cu+2H++NO3-═Cu2++NO↑+H2O |
| B、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O |
| C、过量的二氧化碳通入漂白粉溶液中:ClO-+CO2+H2O═HClO+HCO3- |
| D、AlCl3溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+2H2O+4NH4+ |
20gA物质和14gB物质恰好完全反应,生成8.8gC物质、6.0gD物质和0.2molE物质,则E物质的摩尔质量为( )
| A、100g/mol |
| B、108g/mol |
| C、96g/mol |
| D、55g/mol |
已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为( )
| A、1:3 | B、2:1 |
| C、1:1 | D、1:2 |
对于反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在其他条件不变的情况下( )
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B、改变压强,平衡不发生移动,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量不变 |
| D、对该反应来说,逆反应的速率受温度的影响程度总是大于正反应 |