题目内容
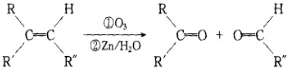
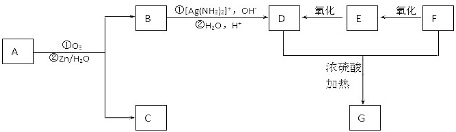
3.烃A可以发生下列过程所示的变化: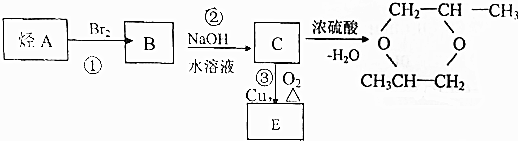
(1)烃A的结构简式是CH2=CHCH3;
(2)反应①属加成反应;
(3)反应②的化学方程式是CH2BrCHBrCH3+2NaOH$→_{△}^{H_{2}O}$CH3CH(OH)CH2OH+2NaBr,属取代或水解反应;
反应③的化学方程式是CH3CH(OH)CH2OH+O2$→_{△}^{Cu}$CH3COCHO+2H2O,属氧化反应.
分析 C发生取代反应生成醚,则C结构简式为CH3CH(OH)CH2OH,C发生催化氧化反应生成E,E结构简式为CH3COCHO,A发生加成反应生成B,B发生水解反应生成C,则A、B结构简式分别为CH2=CHCH3、CH2BrCHBrCH3,结合题目分析解答.
解答 解:C发生取代反应生成醚,则C结构简式为CH3CH(OH)CH2OH,C发生催化氧化反应生成E,E结构简式为CH3COCHO,A发生加成反应生成B,B发生水解反应生成C,则A、B结构简式分别为CH2=CHCH3、CH2BrCHBrCH3,
(1)通过以上分析知,A结构简式为CH2=CHCH3,故答案为:CH2=CHCH3;
(2)反应①属加成反应,故答案为:加成;
(3)卤代烃发生水解反应生成醇,反应②的化学方程式为CH2BrCHBrCH3+2NaOH$→_{△}^{H_{2}O}$CH3CH(OH)CH2OH+2NaBr,属于取代反应或水解反应,
C发生催化氧化反应生成E,反应③的化学方程式是CH3CH(OH)CH2OH+O2$→_{△}^{Cu}$CH3COCHO+2H2O,属于氧化反应,
故答案为:CH2BrCHBrCH3+2NaOH$→_{△}^{H_{2}O}$CH3CH(OH)CH2OH+2NaBr;取代或水解;CH3CH(OH)CH2OH+O2$→_{△}^{Cu}$CH3COCHO+2H2O;氧化.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析判断能力,明确常见有机物结构及其性质、反应条件、反应类型等之间的关系是解本题关键,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
13.采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收.下列说法不正确的是( )
| A. | 在浓海水中存在反应 Br2+H2O?HBr+HBrO | |
| B. | 纯碱溶液显碱性的原因是 CO32-+2H2O?H2CO3+OH- | |
| C. | 海水中提取溴还可用到的反应 Cl2+2Br-═2Cl-+Br2 | |
| D. | 纯碱吸收溴的主要反应是3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑ |
14.化学与材料、能源、环境等密切联系.下列说法不正确的是( )
| A. | 研发光电转换材料,充分利用太阳能 | |
| B. | 包装材料聚氯乙烯属于烃,会造成环境污染 | |
| C. | 用石灰对煤燃烧形成的烟气脱硫,并回收石膏 | |
| D. | 研发高效生物生长调节剂,减少对化肥的使用 |
18. 属于轴烯.可用作有机半导体基质材料的掺杂剂,其同分异构体中含有两个碳碳三键的结构有 ( )
属于轴烯.可用作有机半导体基质材料的掺杂剂,其同分异构体中含有两个碳碳三键的结构有 ( )
 属于轴烯.可用作有机半导体基质材料的掺杂剂,其同分异构体中含有两个碳碳三键的结构有 ( )
属于轴烯.可用作有机半导体基质材料的掺杂剂,其同分异构体中含有两个碳碳三键的结构有 ( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
1. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
(1)已知:①2Cu(s)+$\frac{1}{2}$O2(g)═Cu2O(s);△H=-169kJ•mol-1
②C(s)+$\frac{1}{2}$O2(g)═CO(g);△H=-110.5kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)═CuO(s);△H=-157kJ•mol-1
则方法a发生的热化学方程式是:2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+34.5kJ/mol.
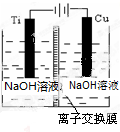
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为阴离子交换膜(填“阴”或“阳”),该电池的阳极反应式为2Cu-2e-+2OH-=Cu2O+H2O,钛极附近的pH值增大(填“增大”“减小”或“不变”).
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
①对比实验的温度:T2>T1(填“>”“<”或“﹦”);
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min).
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O |
| 方法c | 电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑ |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
②C(s)+$\frac{1}{2}$O2(g)═CO(g);△H=-110.5kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)═CuO(s);△H=-157kJ•mol-1
则方法a发生的热化学方程式是:2CuO(s)+C(s)=Cu2O(s)+CO(g)△H=+34.5kJ/mol.
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为阴离子交换膜(填“阴”或“阳”),该电池的阳极反应式为2Cu-2e-+2OH-=Cu2O+H2O,钛极附近的pH值增大(填“增大”“减小”或“不变”).
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
| 序号 | 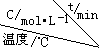 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min).
 +2H2O,反应类型是酯化反应.D与碳酸氢钠反应的化学方程式是HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O.
+2H2O,反应类型是酯化反应.D与碳酸氢钠反应的化学方程式是HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O.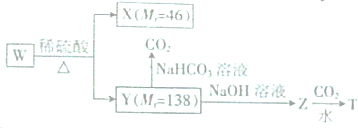
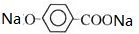 +CO2+H2O→
+CO2+H2O→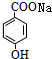 +NaHCO3.
+NaHCO3.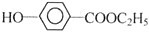
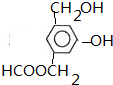 .
.