题目内容
6.向一定量的Fe、FeO和Fe2O3的混合物中,加入120mL 4mol•L-1的稀硝酸,恰好使混合物完全溶解,放出1.344L(标准状况)气体,往所得溶液中加入KMnO4的酸性溶液,无明显现象,若用足量的H2在加热条件下还原相同质量的混合物,最终得到铁的物质的量为( )| A. | 0.21mol | B. | 0.14mol | C. | 0.16mol | D. | 0.24mol |
分析 混合物与硝酸反应时恰好使混合物完全溶解,往所得溶液中加入KMnO4的酸性溶液,无明显现象,说明溶液中的溶质为硝酸铁,由铁元素守恒可知,足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量与硝酸铁中的铁的物质的量相同,根据氮元素守恒求出溶液中硝酸铁的物质的量,即可得到铁的物质的量.
解答 解:因一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol•L-1的稀硝酸,恰好使混合物完全溶解,往所得溶液中加入KMnO4的酸性溶液,无明显现象,说明溶液中的溶质为硝酸铁,1.344LNO(标准状况)的物质的量为:$\frac{1.344L}{22.4L/mol}$=0.06mol,
根据氮元素守恒,硝酸铁中的硝酸根离子的物质的量为:0.12L×4mol/L-0.06mol=0.42mol,
所以硝酸铁的物质的量为:$\frac{1}{3}$×0.42=0.14mol,
由铁元素守恒可知,得到铁的物质的量为n(Fe)=0.14mol,
故选B.
点评 本题考查了有关混合物的计算,侧重考查学生利守恒法计算技巧,题目难度中等,明确硝酸铁与硝酸的关系、硝酸铁中铁元素与原混合物中的铁元素的关系是解答的关键.

练习册系列答案
相关题目
16.元素Y的原子获得3个电子或元素X失去2个电子后,它们的电子层结构与氖原子的相同,X、Y两元素形成的化合物的正确的化学式是( )
| A. | Y3X2 | B. | X2Y3 | C. | X3Y2 | D. | Y2X3 |
17.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.8gD2O 分子中含有的质子数为 NA | |
| B. | 常温下,7.8gNa2O2中含有的阴离子个数为 0.1NA | |
| C. | 标准状况下,11.2L 18O2中所含中子数为 8NA | |
| D. | 25℃时,2.24 LCO2分子中共用电子对数目为 0.4NA |
14.如图是冰部分结构图,下列有关说法正确的是( )


| A. | 因水分子间存在氢键,所以水加热到很高的温度都难以分解 | |
| B. | 1mol 冰中最多含有 4×6.02×1023个氢键,水分子间的氢键可表示为 O-H…O | |
| C. | 在“H2O(s)→H2O(l)→H2+O2”的变化过程中,被破坏的主要作用依次是氢键、极性键 | |
| D. | 等质量的水和冰,因水结冰后氢键数目变少,所以冰的密度比水小 |
1.下列有关说法正确的是( )
| A. | 因为 H-F 的键能大于 H-Cl,所以 HF 沸点高于 HCl | |
| B. | SO3是由极性键构成的非极性分子 | |
| C. | 氯化钠和氯化铯晶体中氯离子的配位数相同 | |
| D. | 第一电离能大小比较 Br>Se>As |
11.下列制取单质的反应中,化合物作还原剂的是( )
| A. | 用锌和稀硫酸反应制取氢气 | B. | 用氢气高温还原氧化铜得到单质铜 | ||
| C. | 用碳和高温水蒸气反应制取氢气 | D. | 用氯气和溴化钠溶液反应制取溴 |
14.将甲烷设计成燃料电池,其利用率更高,如图所示(A,B为多孔性碳棒).持续通入甲烷,在标准状况下,消耗甲烷体积VL,则下列说法错误的是( )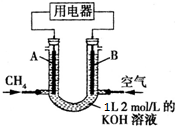

| A. | 通入CH4的一端为原电池的负极,溶液中OH-向负极区移动 | |
| B. | 当0<V≤22.4L时,电池总反应式为CH4+2O2+2KOH═K2CO3+3H2O | |
| C. | 当22.4L<V≤44.8L时,负极电极反应为CH4-8e-+9CO32-+3H2O═10HCO3- | |
| D. | 当V=33.6L时,溶液中阴离子浓度大小关系为c(CO32- )>c(HCO3-)>c(OH-) |