题目内容
17.NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1.8gD2O 分子中含有的质子数为 NA | |
| B. | 常温下,7.8gNa2O2中含有的阴离子个数为 0.1NA | |
| C. | 标准状况下,11.2L 18O2中所含中子数为 8NA | |
| D. | 25℃时,2.24 LCO2分子中共用电子对数目为 0.4NA |
分析 A、求出重水的物质的量,然后根据重水中含10个质子来分析;
B、求出过氧化钠的物质的量,然后根据过氧化钠中含2个钠离子和1个过氧根来分析;
C、求出 18O2的物质的量,然后根据 18O2中含20个中子来分析;
D、二氧化碳所处的状态不明确.
解答 解:A、1.8g重水的物质的量为0.09mol,而重水中含10个质子,故0.09mol重水中含0.9NA个质子,故A错误;
B、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠中含2个钠离子和1个过氧根,故0.1mol过氧化钠中含0.1NA个阴离子,故B正确;
C、标况下11.2L 18O2的物质的量为0.5mol,而 18O2中含20个中子,故0.5mol氧气中含10NA个中子,故C错误;
D、二氧化碳所处的状态不明确,故其物质的量无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.某溶液中可能含有Na+、Mg2+、Fe2+、H+、OH-、NO3-等几种离子中的若干种,向该溶液中加入氧化铝后,溶液中有X离子生成,下列判断中正确的是( )
| A. | 溶液中可以同时含有Fe2+、NO3- | B. | 溶液中一定有OH-、Na+ | ||
| C. | 溶液中可能含有Na+、H+、Mg2+、NO3- | D. | 若X是AlO2-,则上述离子最多有2种 |
12.某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子组合是( )
| A. | Mg2+ | B. | Mg2+、Fe2+ | C. | Fe2+ | D. | Mg2+、Al3+ |
2.在周期表主族元素中,X 元素位于第二周期,且分别与 Y、Z、W 三元素相邻,X、Y 的原子序数之和等于 Z的原子序数;这四种元素原子的最外层电子数之和为 20.下列判断正确的是( )
| A. | 原子序数:Z>Y>X>W | |
| B. | X、Y、Z、W 形成的单质最多有 6 种 | |
| C. | X 元素最高价氧化物对应水化物的化学式为:H3XO4 | |
| D. | 四种元素的气态氢化物中,W 的气态氢化物最稳定 |
6.向一定量的Fe、FeO和Fe2O3的混合物中,加入120mL 4mol•L-1的稀硝酸,恰好使混合物完全溶解,放出1.344L(标准状况)气体,往所得溶液中加入KMnO4的酸性溶液,无明显现象,若用足量的H2在加热条件下还原相同质量的混合物,最终得到铁的物质的量为( )
| A. | 0.21mol | B. | 0.14mol | C. | 0.16mol | D. | 0.24mol |
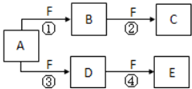 X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示:
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍.A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示: .
.