题目内容
7.X、Y、Z、W均为短周期主族元素,原子序数依次增加,且最外层电子数分别为5、6、6、7,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | 阴离子的还原性:Z>Y | |
| B. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| C. | Z的单质与氢气反应较Y剧烈 | |
| D. | X、Y形成的化合物都易溶于水 |
分析 X、Y、Z、W均为短周期主族元素,原子序数依次增加,且最外层电子数分别为5、6、6、7;若Y原子的最外层电子数是内层电子数的3倍,最外层最多容纳8个电子,则Y含有2个电子层,最外层含有6个电子,为O元素;Z的原子序数大于O,最外层含有6个电子,只能为S元素;W为短周期元素,原子序数大于S,为Cl元素;X最外层含有5个电子,原子序数小于O,为N元素,据此结合元素周期律知识解答.
解答 解:X、Y、Z、W均为短周期主族元素,原子序数依次增加,且最外层电子数分别为5、6、6、7;若Y原子的最外层电子数是内层电子数的3倍,最外层最多容纳8个电子,则Y含有2个电子层,最外层含有6个电子,为O元素;Z的原子序数大于O,最外层含有6个电子,只能为S元素;W为短周期元素,原子序数大于S,为Cl元素;X最外层含有5个电子,原子序数小于O,为N元素,
A.Y为O、Z为S元素,硫元素的非金属性比氧元素弱,所以简单阴离子的还原性Z>Y,故A正确;
B.W的最高价氧化物对应水化物为HClO4,Z的最高价氧化物对应水化物为H2SO4,HClO4酸性比H2SO4强,故B错误;
C.非金属性:O>S,则O2与氢气反应比S剧烈,故C错误;
D.X、Y可以形成不溶于水的化合物,如NO,故D错误;
故选A.
点评 本题考查了原子结构与元素周期律的应用,题目难度中等,正确推断元素为解答关键,注意熟练掌握元素周期表结构、元素周期律内容,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 | |
| B. | 棉、丝、羽毛、塑料及合成橡胶完全燃烧都只生成CO2和H2O | |
| C. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| D. | 新型材料聚酯纤维、光导纤维都属于有机高分子化合物 |
2. 常温下,向20.00mL 0.1mol•L-1的MOH溶液中逐滴加入一定浓度的HA溶液.滴加过程中,溶液的pH与滴入HA溶液的体积关系如图所示,当pH=8时MOH溶液恰好被中和.则下列说法中错误的是( )
常温下,向20.00mL 0.1mol•L-1的MOH溶液中逐滴加入一定浓度的HA溶液.滴加过程中,溶液的pH与滴入HA溶液的体积关系如图所示,当pH=8时MOH溶液恰好被中和.则下列说法中错误的是( )
 常温下,向20.00mL 0.1mol•L-1的MOH溶液中逐滴加入一定浓度的HA溶液.滴加过程中,溶液的pH与滴入HA溶液的体积关系如图所示,当pH=8时MOH溶液恰好被中和.则下列说法中错误的是( )
常温下,向20.00mL 0.1mol•L-1的MOH溶液中逐滴加入一定浓度的HA溶液.滴加过程中,溶液的pH与滴入HA溶液的体积关系如图所示,当pH=8时MOH溶液恰好被中和.则下列说法中错误的是( )| A. | ②点混合溶液中水电离出的c(H+)大于酸HA溶液中由水电离出的c(H+) | |
| B. | ③点混合溶液中各离子浓度的大小关系是c(M+)=c(A-)>c(H+)=c(OH-) | |
| C. | 酸HA溶液的浓度为0.1 mol•L-1 | |
| D. | ④点溶液中,存在c(HA)+c(H+)>c(M+)+c(OH-) |
16.下列装置图中的实验方案,能达到实验目的是( )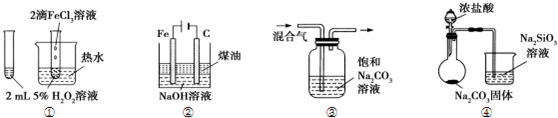

| A. | ①验证FeCl3对H2O2分解反应有催化作用 | |
| B. | ②制备Fe(OH)2并能较长时间观察其颜色 | |
| C. | ③除去CO2气体中混有的SO2 | |
| D. | ④比较HCl、H2CO3和H2SiO3的酸性强弱 |
17.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 在标准状况下,0.5 molNO与0.5 molO2混合后气体分子数为0.75 NA | |
| B. | 某温度下纯水的pH=6,该温度下10 L pH=11的NaOH溶液中含OH-的数目为NA | |
| C. | 0.1molAlCl3完全转化为氢氧化铝胶体,生成O.l NA个胶体粒子 | |
| D. | 以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子,则正极放出H2的体积为11.2 L |
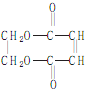 )的合成路线如下图:
)的合成路线如下图: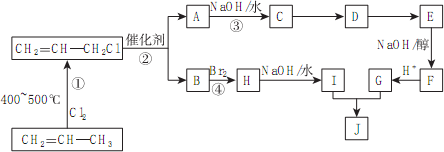
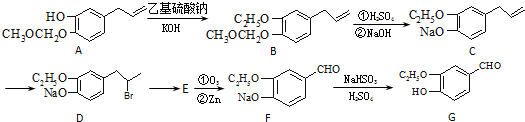
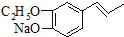 .
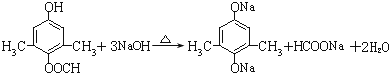
.
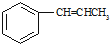 为原料制备
为原料制备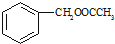 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: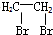


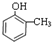 .
.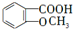 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$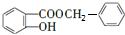 +HCl.
+HCl.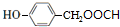 .
.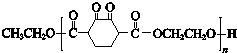 )是人造棉的主要成分之一,合成路线如下:
)是人造棉的主要成分之一,合成路线如下: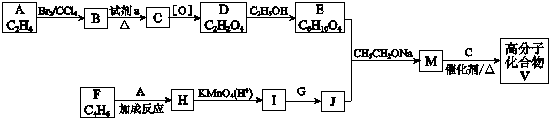
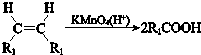
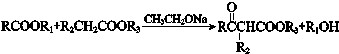 (R、R1、R2、R3表示烃基)
(R、R1、R2、R3表示烃基)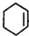 .
.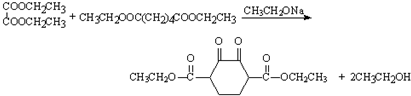 .
. .
.