题目内容
下列说法或表示法错误的是( )
| A、化学反应过程中的能量变化除了热能外,还可以是光能、电能等 |
| B、放热反应的△H<0 |
| C、需要加热才能发生反应一定是吸热反应 |
| D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、根据化学反应过程中的能量变化形式分析;
B、放热反应的△H<0;
C、部分放热反应也需要反应条件;
D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数.
B、放热反应的△H<0;
C、部分放热反应也需要反应条件;
D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数.
解答:
解:A、根据化学反应过程中的能量转化形式分析,除了热能外,也可以是光能、电能等,故A正确;
B、放热反应的△H<0,故B正确;
C、有的放热反应也需要加热才能进行,如木材的燃烧,故C错误;
D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数,故D 正确;
故选C.
B、放热反应的△H<0,故B正确;
C、有的放热反应也需要加热才能进行,如木材的燃烧,故C错误;
D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数,故D 正确;
故选C.
点评:本题主要考查了放热与吸热反应的原因、常见的吸热和放热反应,是对基本知识的考查,较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
近年来科学家正在研制一种高容量、低成本锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )| A、放电时,Li+透过固体电解质向Cu极移动 |
| B、放电时,负极的电极反应式为CuO+H2O+2e---Cu+2OH- |
| C、通空气时,铜被腐蚀,表面产生Cu2O |
| D、整个反应过程中,铜相当于催化剂 |
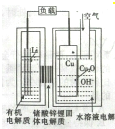
 生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池.其工作原理如图所示.下列有关说法正确的是( )
生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池.其工作原理如图所示.下列有关说法正确的是( )| A、、O2在C2电极上得电子,被氧化 |
| B、电子由C2极经外电路流向C1极 |
| C、每转移6mole-1,理论上生成22.4LCO2 |
| D、C1极的电极反应式为:C2H5OH+3H2O-12e-1=2CO2+12H+ |
下列现象与胶体知识无关的是( )
| A、日常生活中看到的云、烟、雾 |
| B、蒸发饱和食盐水析出氯化钠晶体 |
| C、向豆浆中加入盐卤做豆腐 |
| D、光线射入蛋白质溶液里,形成光亮的通路 |
设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA |
| B、常温常压下,18 g H2O 中含有的原子总数为3NA |
| C、1 L 0.1 mol?L-1NaHCO3液含有0.1NA个HCO3- |
| D、常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA |