题目内容
设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA |
| B、常温常压下,18 g H2O 中含有的原子总数为3NA |
| C、1 L 0.1 mol?L-1NaHCO3液含有0.1NA个HCO3- |
| D、常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA |
考点:阿伏加德罗常数
专题:
分析:A、氯气溶于水部分与水反应;
B、18个水的物质的量为1mol,1mol水中含有3mol原子;
C、HCO3-既能电离又能水解;
D、常温常压下,不能使用标况下的气体摩尔体积计算混合气体的物质的量.
B、18个水的物质的量为1mol,1mol水中含有3mol原子;
C、HCO3-既能电离又能水解;
D、常温常压下,不能使用标况下的气体摩尔体积计算混合气体的物质的量.
解答:
解:A、标准状况下,2.24L Cl2物质的量为0.1mol,溶于水部分和水反应,转移的电子数目小于0.1NA,故A错误;
B、水的摩尔质量为18g/mol,18g水的物质的量为1mol,1mol水中含有3mol原子,含有的原子总数为3NA,故B正确;
C、HCO3-既能电离又能水解,故溶液中的HCO3-个个数小于0.1NA个,故C错误;
D、不是标况下,不能使用标况下的气体摩尔体积计算2.24L混合气体的物质的量,故D错误;
故选B.
B、水的摩尔质量为18g/mol,18g水的物质的量为1mol,1mol水中含有3mol原子,含有的原子总数为3NA,故B正确;
C、HCO3-既能电离又能水解,故溶液中的HCO3-个个数小于0.1NA个,故C错误;
D、不是标况下,不能使用标况下的气体摩尔体积计算2.24L混合气体的物质的量,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
下列事实不能说明醋酸为弱酸的是( )
| A、稀醋酸溶液的导电性比较弱 |
| B、向CH3COONa溶液中滴入酚酞试液,溶液变红色 |
| C、一定温度下,向某醋酸溶液中加入CH3COONH4晶体,溶液pH增大 |
| D、一定温度下,向体积相同,pH值也相同的盐酸和醋酸中,投入相同质量的锌粒,锌粒完全溶解所消耗的时间不同 |
下列说法或表示法错误的是( )
| A、化学反应过程中的能量变化除了热能外,还可以是光能、电能等 |
| B、放热反应的△H<0 |
| C、需要加热才能发生反应一定是吸热反应 |
| D、热化学方程式中的化学计量数仅表示该物质的物质的量,可以是分数 |
一只盛有CO、O2、N2混合气体的气球放在空气(空气平均摩尔质量为29g/mol)中静止不动,则混合气体中O2的体积分数是( )
| A、75% | B、25% |
| C、50% | D、无法计算 |
下列有关化学与生活、生产的叙述错误的是( )
| A、因为氮易液化,液氮在气化时会吸收大量的热量,所以液氮可作制冷剂 |
| B、盐卤点豆腐,明矾净水与胶体的性质有关 |
| C、H2O2、SO2、O3等都用于织物漂白,它们的漂白原理相同 |
| D、硫酸和硝酸都是重要的工业原料,工业上可用于制化肥、农药和炸药 |
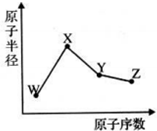 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强,下列说法正确的是( )| A、对应气态氢化物的稳定性Y>Z |
| B、化合物XZW既含离子键也含共价键 |
| C、对应简单离子半径W<X |
| D、Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |

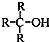 )不能氧化成醛或酮.
)不能氧化成醛或酮.