题目内容
4.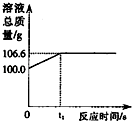 将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答:
将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答:(1)通入的CO2的质量为6.6g;
(2)计算氢氧化钠溶液的溶质质量分数;
(3)实验结束后所得不饱和溶液的质量.
分析 (1)CO2和NaOH反应时生成Na2CO3,溶液质量增加的质量为CO2质量;
(2)根据二氧化碳和NaOH之间的关系式计算n(NaOH),其质量分数=$\frac{m(NaOH)}{NaOH溶液质量}$×100%;
(3)图中溶液最终质量为不饱和溶液质量.
解答 解:(1)CO2和NaOH反应时生成Na2CO3,溶液质量增加的质量为CO2质量=(106.6-100.0)g=6.6g,
故答案为:6.6;
(2)二氧化碳和NaOH反应方程式为CO2+2NaOH=Na2CO3+H2O,根据方程式知,参加反应的n(NaOH)=2n(CO2)=2×$\frac{6.6g}{44g/mol}$=0.3mol,NaOH的质量分数=$\frac{m(NaOH)}{NaOH溶液质量}$×100%=$\frac{40g/mol×0.3mol}{100g}$×100%=12%,
答:NaOH溶液的质量分数为12%;
(3)图中溶液最终质量为不饱和溶液质量,其质量为106.6g,
答:不饱和溶液的质量为106.6g.
点评 本题考查化学方程式的有关计算,为高频考点,侧重考查学生分析计算能力,明确NaOH和二氧化碳之间的关系式及图中溶液质量变化关系是解本题关键,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
1.下列叙述中不正确的是( )
| A. | 电镀时,电镀池里的阳极材料发生氧化作用 | |
| B. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| C. | 惰性电极电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
15.某种解热镇痛药的结构简式如图所示,当它完全水解时,不可能得到的产物是( )
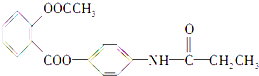
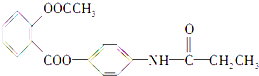
| A. | CH3CH2COOH | B. | CH3COOH | C. | CH3OH | D. | 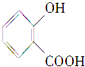 |
19.自然界中存在一种尖晶石,化学式可表示为MgAl2O4.已知某尖晶石样品中混有Fe2O3,取5.4g该样品,恰好完全溶解于100g一定浓度的盐酸,则该盐酸的质量分数可能为( )
| A. | 6.5% | B. | 8.5% | C. | 11.5% | D. | 12.5% |
9.体积相同、浓度相同的HCl溶液和CH3COOH溶液分别与足量的锌粒(假设锌粒的颗粒大小相同,质量也相同)反应,下列有关说法正确的是( )
| A. | 生成氢气是HCl溶液多 | |
| B. | 生成氢气是CH3COOH溶液多 | |
| C. | 反应速率是HCl溶液与锌反应的快 | |
| D. | 反应速率是CH3COOH溶液与锌反应的快 |
13.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
| A. | 第一块钠消耗的氧气多 | B. | 两块钠消耗的氧气一样多 | ||
| C. | 第二块钠的反应产物质量大 | D. | 两块钠的反应产物质量一样大 |