题目内容
1.下列叙述中不正确的是( )| A. | 电镀时,电镀池里的阳极材料发生氧化作用 | |
| B. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| C. | 惰性电极电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 | |
| D. | 电解熔融的氧化铝制取金属铝,用铁作阳极 |
分析 A、电镀时,阳极上失电子发生氧化反应;
B、铁为活性电极,电解饱和食盐水,涂镍碳钢网应为阴极;
C、电解氯化铜溶液,阳极上生成氯气,阴极上生成铜,依据电子守恒计算产物物质的量之比;
D、电解熔融的氧化铝制取金属铝,用铁作阳极.
解答 解:A、电镀时,阳极上电极材料失电子发生氧化反应,故A正确;
B、铁为活性电极,电解饱和食盐水,涂镍碳钢网应为阴极,在阳极可生成氯气,在阴极生成氢气和氢氧化钠溶液,故B正确;
C、电解氯化铜溶液,阳极上生成氯气,电极反应为:2Cl--2e-=Cl2↑,阴极上生成铜,电极反应为:Cu2++2e-=Cu,依据电子守恒计算在阴极上和阳极上析出的产物的物质的量之比为1:1,故C正确;
D、电解原理分析,铁做阳极失电子溶解不符合生产实际,电解熔融的氧化铝制取金属铝,用石墨作阳极,故D错误.
故选D.
点评 本题考查学生电解池的工作原理,主要是电解精炼铜、电镀、氯碱工业原理分析判断,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.某无色气体可能含有甲烷、一氧化碳、氢气中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全):
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
①无色气体在足量氧气中燃烧;
②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6克;
③再将剩余气体通过盛有澄清石灰水溶液的洗气瓶,装置增重4.4克.下列推断正确的是( )
| A. | 该气体可能只含有一氧化碳、氢气 | B. | 该气体可能只含有甲烷、一氧化碳 | ||
| C. | 该气体一定只含有甲烷 | D. | 该气体一定只含有甲烷、氢气 |
9.常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是( )
| A. | C2H5OH | B. | CH4 | C. | C2H4O | D. | C3H8 |
16.室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是( )
| A. | 0.1mol/L的盐酸和0.1mol/L的氨水溶液 | |
| B. | 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液 | |
| C. | pH=4的醋酸溶液和pH=10的氢氧化钠溶液 | |
| D. | pH=4的盐酸和pH=l0的氨水 |
13.下列反应的化学方程式正确的是( )
| A. | 乙烯和溴单质反应:CH2═CH2+Br2→CH2-CH2Br2 | |
| B. | 合成聚乙烯塑料:nCH2═CH2→ | |
| C. | 皂化反应: +3H2O$→_{△}^{H+}$ +3H2O$→_{△}^{H+}$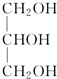 +3C17H35COOH +3C17H35COOH | |
| D. | 乙醇与金属钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
3.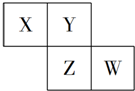 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X、Y、Z、W元素的氢化物分子间都可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |
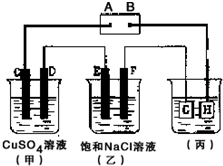 如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题:
如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题: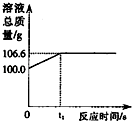 将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答:
将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答: