题目内容
9.体积相同、浓度相同的HCl溶液和CH3COOH溶液分别与足量的锌粒(假设锌粒的颗粒大小相同,质量也相同)反应,下列有关说法正确的是( )| A. | 生成氢气是HCl溶液多 | |
| B. | 生成氢气是CH3COOH溶液多 | |
| C. | 反应速率是HCl溶液与锌反应的快 | |
| D. | 反应速率是CH3COOH溶液与锌反应的快 |
分析 盐酸是强酸完全电离,醋酸是弱酸不完全电离,相同体积相同浓度的盐酸和醋酸的物质的量相同,与足量Zn反应生成氢气的物质的量相同,但醋酸溶液中氢离子浓度小,开始反应速率慢,据此分析.
解答 解:相同体积相同浓度的盐酸和醋酸的物质的量相同,与足量Zn反应生成氢气的物质的量相同,盐酸是强酸完全电离,醋酸是弱酸不完全电离,醋酸溶液中氢离子浓度小,开始反应速率慢,
故选C.
点评 本题考查了弱电解质的电离,不同的一元酸中和碱时,消耗碱的物质的量与酸的物质的量有关,与酸的强弱无关,为易错点.

练习册系列答案
相关题目
14.向Na2CO3溶液中逐滴滴入稀盐酸,溶液中的HCO3-浓度的变化情况是( )
| A. | 逐渐增大 | B. | 逐渐减小 | ||
| C. | 先逐渐增大后减小 | D. | 先逐渐减小后增大 |
18.下列离子方程式书写正确的是( )
| A. | 过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 | |
| B. | 铜片与稀硝酸反应:Cu+NO3-+4H+=Cu2++NO↑+2H2O | |
| C. | Fe2(SO4)3的酸性溶液中通入足量硫化氢Fe3++H2S=Fe2++S↓+2H+ | |
| D. | 在碳酸氢钙溶液中加入过量氢氧化钠溶液Ca2++HCO3-+OH-=CaCO3↓+H2O |
19.已知BF3分子的空间构型为平面三角形,用等电子原理判断,下列分子或离子的立体构型不是平面三角形的是( )
| A. | SO3 | B. | PCl3 | C. | NO3- | D. | BCl3 |
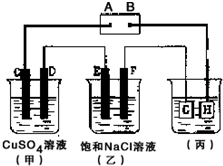 如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题:
如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题: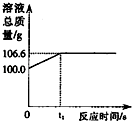 将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答:
将一定量的CO2通入100g氢氧化钠溶液中恰好完全吸收,形成不饱和溶液,该溶液总质量与反应时间的变化关系如图.试分析解答: