题目内容
已知常温下:
KSP[Mg(OH)2]=1.2×10-11mol3?L-3
KSP(AgCl)=1.8×10-10mol2?L-2
KSP(Ag2CrO4)=1.9×10-12mol3?L-3
KSP(CH3COOAg)=2.3×10-3mol-2?L-2
下列叙述正确的是( )
KSP[Mg(OH)2]=1.2×10-11mol3?L-3
KSP(AgCl)=1.8×10-10mol2?L-2
KSP(Ag2CrO4)=1.9×10-12mol3?L-3
KSP(CH3COOAg)=2.3×10-3mol-2?L-2
下列叙述正确的是( )
| A、等体积混合浓度均为0.2mol/L的AgNO3溶液和CH3COONa溶液不一定产生CH3COOAg沉淀 |
| B、将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4溶液中先产生Ag2CrO4沉淀 |
| C、在Mg2+为0.12mol/L的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上 |
| D、向饱和AgCl水溶液中加入NaCl溶液,KSPAgCl变大 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、根据Ksp(CH3COOAg)=c(CH3COO-)×c(Ag+)计算;
B、根据Ksp(AgCl)以及Ksp(Ag2CrO4),当离子的浓度幂之积大于溶度积时,生成沉淀;
C、根据Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)计算;
D、Ksp(AgCl)只受温度的影响.
B、根据Ksp(AgCl)以及Ksp(Ag2CrO4),当离子的浓度幂之积大于溶度积时,生成沉淀;
C、根据Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)计算;
D、Ksp(AgCl)只受温度的影响.
解答:
解:A、等体积混合浓度均为0.2mol?L-1,c(CH3COO-)×c(Ag+)=0.04>2.3×10-3,一定产生CH3COOAg沉淀,故A错误;
B、将0.001 mol?L-1的AgNO3溶液滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4溶液中,c(Ag+)×c(Cl-)=10-6,c2(Ag+)×c(CrO42-)=10-9,AgCl先达到饱和,应先生成AgCl沉淀,故B错误;
C.Ksp〔Mg(OH)2〕=c(Mg2+)×c2(OH-),c(OH-)≥
=10-5 mol?L-1,溶液的pH至少要控制在9以上,故C正确;
D.Ksp(AgCl)只受温度的影响,与浓度无关,故D错误.
故选C.
B、将0.001 mol?L-1的AgNO3溶液滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4溶液中,c(Ag+)×c(Cl-)=10-6,c2(Ag+)×c(CrO42-)=10-9,AgCl先达到饱和,应先生成AgCl沉淀,故B错误;
C.Ksp〔Mg(OH)2〕=c(Mg2+)×c2(OH-),c(OH-)≥
|
D.Ksp(AgCl)只受温度的影响,与浓度无关,故D错误.
故选C.
点评:本题综合考查难溶电解质的溶解平衡,侧重于计算,题目难度中等,注意把握计算公式的应用易错选A.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案
相关题目
下列有关表述正确的是( )
A、次氯酸的电子式: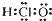 |
B、N原子的电子排布图: |
| C、硫原子的价电子排布式:3s23p4 |
| D、氯化钠的分子式:NaCl |
下列叙述正确的是( )
| A、可以根据PbI2和AgCl的Ksp的大小比较两者的溶解度 |
| B、常温下,同浓度的Na2S与NaHS溶液相比,NaHS溶液的pH大 |
| C、等物质的量浓度的CH3COONH4溶液和NH4HSO4溶液,前者的c(NH4+)小 |
| D、用惰性电极电解饱和NaCl溶液,若有1.0 mol电子转移,则理论生成1.0 mol NaOH |
对已达平衡的反应2X(g)+Y(g)?4Z(g),改变以下哪种条件能使速率变化如图所示( )


| A、增大Z的浓度 |
| B、减小X的浓度 |
| C、增大压强 |
| D、减小压强 |
已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,现取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀平衡时,测得溶液的pH=13,则下列说法不正确的是( )
| A、所得溶液中由水离出的C(OH-)=1.0×10-13mol?L-1 |
| B、所加烧碱溶液的pH=13 |
| C、所得溶液中C(Mg2+)=5.6×10-10mol?L-1 |
| D、在整个反应过程中,H2O的电离度在逐渐减小 |
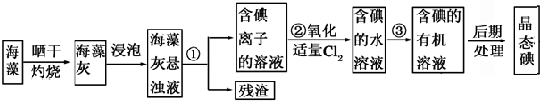



 一定条件下聚合生成一种合成纤维:
一定条件下聚合生成一种合成纤维: .
. 在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等离子.试分析回答下列问题:
在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中含有大量Mg2+、Al3+、Fe3+、Ag+、Ba2+等离子.试分析回答下列问题: