题目内容
下列有关表述正确的是( )
A、次氯酸的电子式: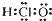 |
B、N原子的电子排布图: |
| C、硫原子的价电子排布式:3s23p4 |
| D、氯化钠的分子式:NaCl |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.次氯酸的中心原子为氧原子,其分子中不存在氢氯键;
B.N原子核外电子数为7,处于2p能级上的3个电子应尽可能分占3个不同2p原子轨道,且自旋状态相同,因此违背了洪特规则;
C.硫原子核外含有3个电子层,最外层含有6个电子,据此写出其价电子排布式;
D.氯化钠为离子化合物,不存在分子式,NaCl为化学式.
B.N原子核外电子数为7,处于2p能级上的3个电子应尽可能分占3个不同2p原子轨道,且自旋状态相同,因此违背了洪特规则;
C.硫原子核外含有3个电子层,最外层含有6个电子,据此写出其价电子排布式;
D.氯化钠为离子化合物,不存在分子式,NaCl为化学式.
解答:
解:A.次氯酸中存在1个氢氧键和1个氧氯键,分子中不存在氢氯键,次氯酸正确的电子式为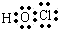 ,故A错误;
,故A错误;
B.N原子核外有7个电子,分别位于1S、2S、2P轨道,其正确的轨道表示式为 ,故B错误;
,故B错误;
C.硫原子的核外电子总数为16,最外层为6个电子,则硫原子的价电子排布式为:3s23p4,故C正确;
D.氯化钠属于离子化合物,NaCl为氯化钠的化学式,氯化钠不存在分子式,故D错误;
故选C.
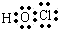 ,故A错误;
,故A错误;B.N原子核外有7个电子,分别位于1S、2S、2P轨道,其正确的轨道表示式为
 ,故B错误;
,故B错误;C.硫原子的核外电子总数为16,最外层为6个电子,则硫原子的价电子排布式为:3s23p4,故C正确;
D.氯化钠属于离子化合物,NaCl为氯化钠的化学式,氯化钠不存在分子式,故D错误;
故选C.
点评:本题考查了常见化学用语的表示方法判断,题目难度中等,注意掌握电子式、轨道排布式、电子排布式、化学式与分子式等化学用语的概念及表示方法,明确分子数与化学式的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
制造太阳能电池需要高纯度的硅,工业上制高纯度硅常用以下反应来实现:(1)Si(粗)+3HCl
SiHCl3+H2,(2)SiHCl3+H2
Si+3HCl.对上述两个反应的叙述中,错误的是( )
| ||
| ||
| A、两个反应都是置换反应 |
| B、两个反应中的H2均为还原剂 |
| C、两个反应的条件不同 |
| D、两个反应都是氧化还原反应 |
下列物质的沸点逐渐升高的是( )
| A、NH3 PH3 AsH3 SbH3 |
| B、CH4 SiH4 GeH4 SnH4 |
| C、CI4 CBr4 CF4 CCl4 |
| D、HF HCl HBr HI |
下列说法正确的是( )
| A、相同体积和物质的量浓度的不同溶液里所含溶质的物质的量相同 | ||
| B、10mol/L的浓盐酸与H2O等质量混合所得混合液的浓度为5mol/L | ||
C、溶液中溶质质量分数为w,密度为ρg?cm-3,溶质摩尔质量为Mg?mol-1的溶液的物质的量浓度为
| ||
| D、一定物质的量浓度的溶液配制过程中,仰视定容,所得溶液的浓度偏大 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA |
| B、0.1mol苯中含有双键的数目为0.3NA |
| C、标准状况下,22.4L乙醇中含有分子的数目为NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
设nA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温常压下,8gO2含有2nA个电子 |
| B、10L0.1mol?L-1的氨水中有nA个NH4+ |
| C、标准状况下,22.4L盐酸含有nA个HCl分子 |
| D、1molNa与足量氧气反应生成Na2O和Na2O2的混合物,失去nA个电子 |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与盐酸的反应 2OH-+2H+=2H2O |
| B、钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag |
| D、碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
已知常温下:
KSP[Mg(OH)2]=1.2×10-11mol3?L-3
KSP(AgCl)=1.8×10-10mol2?L-2
KSP(Ag2CrO4)=1.9×10-12mol3?L-3
KSP(CH3COOAg)=2.3×10-3mol-2?L-2
下列叙述正确的是( )
KSP[Mg(OH)2]=1.2×10-11mol3?L-3
KSP(AgCl)=1.8×10-10mol2?L-2
KSP(Ag2CrO4)=1.9×10-12mol3?L-3
KSP(CH3COOAg)=2.3×10-3mol-2?L-2
下列叙述正确的是( )
| A、等体积混合浓度均为0.2mol/L的AgNO3溶液和CH3COONa溶液不一定产生CH3COOAg沉淀 |
| B、将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4溶液中先产生Ag2CrO4沉淀 |
| C、在Mg2+为0.12mol/L的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上 |
| D、向饱和AgCl水溶液中加入NaCl溶液,KSPAgCl变大 |