题目内容
16.下列变化中,加入铁粉不可能实现的是( )| A. | Ag+→Ag | B. | Fe3+→Fe2+ | C. | H+→H2 | D. | Fe(OH)2→Fe(OH)3 |
分析 A、银离子与铁粉发生氧化还原反应;
B、铁离子与单质铁发生归中反应;
C、铁与非氧化性的酸发生氧化还原反应;
D、氢氧化亚铁转化为氢氧化铁是发生氧化反应,而铁是还原剂,所以氢氧化亚铁与铁不反应.
解答 解;A、银离子与铁粉发生氧化还原反应,如铁与硝酸银溶液反应生成单质银,故A不选;
B、铁离子与单质铁发生归中反应,铁与氯化铁反应生成氯化亚铁,故B不选;
C、铁与非氧化性的酸发生氧化还原反应,铁与盐酸反应生成氯化亚铁与氢气,故C不选;
D、氢氧化亚铁转化为氢氧化铁是发生氧化反应,而铁是还原剂,所以氢氧化亚铁与铁不反应,所以不能实现,故D选;
故选D.
点评 本题考查氧化还原反应和铁的化学性质,学生要清楚氢氧化亚铁转化为氢氧化铁是发生氧化反应,应添加氧化剂,而 铁是还原剂,比较容易.

练习册系列答案
相关题目
7.将0.1mol下列物质置于1L水中,充分搅拌后,溶液中阴离子数最多的是( )
| A. | KBr | B. | Mg(OH)2 | C. | Na2CO3 | D. | MgSO4 |
4.下列有关物质的用途叙述不正确的是( )
| A. | 氧化铁通常用作红色油漆和涂料 | |
| B. | 用铝制餐具长期存放碱性食物 | |
| C. | 过氧化钠可以用作潜水艇里氧气的来源 | |
| D. | 硅可用于制作电脑芯片 |
11.现有20.0g某铁矿石样品(主要成分为Fe2O3和FeO).粉碎后加入足量盐酸(假设杂质不与盐酸反应),充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤,将所得沉淀在空气中蒸干并灼烧,冷却后称得固体质量为16.0g,则该铁矿石样品中铁元素的质量分数为( )
| A. | 28% | B. | 56% | C. | 72% | D. | 80% |
1.反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.下列叙述不正确的是( )
| A. | 氧化剂为KMnO4,其中Cl元素被还原 | |
| B. | 若有0.8molH2O生成,则反应中有NA个电子转移 | |
| C. | 浓HCl在反应中起酸性和还原性的作用 | |
| D. | 由此反应可以大胆推测氧化性强弱关系:KMnO4>MnO2 |
8.短周期元素A、B、C的原子序数依次增大,其原子的最外层电子数之和为10,且A与C在周期表中位置上下相邻,B原子最外层电子数等于A原子次外层电子数,下列有关叙述不正确的是( )
| A. | 原子半径:A<B<C | |
| B. | A的氢化物的稳定性大于C的氢化物的稳定性 | |
| C. | A的最高价氧化物与B的单质可以发生置换反应 | |
| D. | C的氧化物的熔点比A的氧化物熔点低 |
5.下列化合物中,能通过单质与酸反应或单质间化合直接制取的是( )
| A. | CuCl2 | B. | FeCl2 | C. | AlCl3 | D. | FeCl3 |
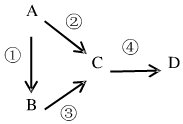 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.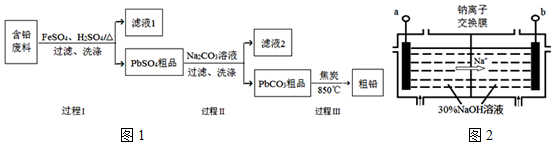
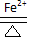 2PbSO4+2H2O.
2PbSO4+2H2O.