题目内容
已知Ksp(AgC1)=1.8×10-10mol2?L-2,Ksp(AgI)=1.0×1016mo2?L-2.下列说法错误的是( )
| A、AgCl不溶于水,不能转化为AgI | ||||
| B、在含浓度均为0.001mol?L-1的Cl-、I-的溶液中缓慢滴AgNO3稀溶液,先析出AgI | ||||
| C、AgI比AgCl更难溶于水,所以AgCl可转化为AgI | ||||
D、常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于
|
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.AgCl能转化为AgI;
B.根据溶解度小的物质先生成沉淀;
C.根据沉淀转化原理分析;
D.根据Ksp(AgCl)求出c(Ag+),再利用Ksp(AgI)求出碘离子的浓度.
B.根据溶解度小的物质先生成沉淀;
C.根据沉淀转化原理分析;
D.根据Ksp(AgCl)求出c(Ag+),再利用Ksp(AgI)求出碘离子的浓度.
解答:
解:A.AgCl难溶,但是AgI溶解度更小,所以AgCl能转化为AgI,故A错误;
B.在含浓度均为0.001mol?L-1的Cl-、I-的溶液中缓慢滴AgNO3稀溶液,由于AgI的溶度积小,即溶解度小,所以AgI先形成沉淀析出,故B正确;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的,所以AgCl可以转化为AgI,故C正确;
D.已知Ksp(AgCl)=1.8×10-10,则c(Ag+)=
=
,c(I-)=
=
=
×10-11mol/L,故D正确;
故选:A.
B.在含浓度均为0.001mol?L-1的Cl-、I-的溶液中缓慢滴AgNO3稀溶液,由于AgI的溶度积小,即溶解度小,所以AgI先形成沉淀析出,故B正确;
C.根据沉淀转化原理:溶解度小的能转化为溶解度更小的,所以AgCl可以转化为AgI,故C正确;
D.已知Ksp(AgCl)=1.8×10-10,则c(Ag+)=
| Ksp(AgCl) |
| 1.8×10-10 |
| Ksp(AgI) |
| c(Ag+) |
| 1.0×10-16 | ||
|
| 1 | ||
|
故选:A.
点评:本题考查难溶电解质的溶解平衡及沉淀转化的本质,注意沉淀转化为溶解度更小的物质容易发生,题目难度不大.

练习册系列答案
相关题目
相同温度时,有关①100mL 0.1mol/L NaHCO3②100mL 0.1mol/L Na2CO3两种溶液的叙述不正确的是( )
| A、①溶液中:c(CO32-)<c(H2CO3) |
| B、溶液的pH:②>① |
| C、溶液中的阴离子种类:②>① |
| D、②溶液中:c(HCO3-)>c(H2CO3) |
一位患者镶了两颗假牙,其中一颗是黄金的,另一颗是不锈钢的.自镶上假牙后,他时感头疼,心情烦躁,多次治疗未见好转.如果你是医生,下列方法不能治疗其疾病的是( )
| A、将两颗假牙都做成黄金的 |
| B、将两颗假牙都做成不锈钢的 |
| C、将两颗假牙都做成特殊树脂的 |
| D、将金假牙改为铝质假牙 |
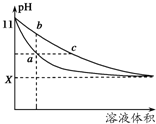 某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
某温度下,相同体积、相同pH的氨水和氢氧化钠溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )| A、a点导电能力比b点强 |
| B、对于b、c两点,Kb>Kc |
| C、与盐酸完全反应时,消耗盐酸体积Va>Vc |
| D、X的值接近7,但大于7 |
NA表示阿伏加德罗常数的值.下列说法中,正确的是( )
| A、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA |
| B、电解精炼铜时,当电路中转移NA个电子,阳极溶解32g铜 |
| C、向仅含0.2molFeI2的溶液中持续通入氯气,当有0.1molFe2+被氧化时,转移电子的数目为0.5NA |
| D、将100 mL0.1mol?L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA |
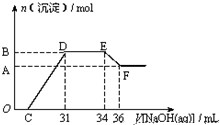 某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )
某同学取一定量Fe与Al的混合物与一定量极稀的硝酸充分反应,已知硝酸的还原产物仅有一种,在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示,试分析硝酸被还原后生成的产物为( )| A、NH4NO3 |
| B、NO2 |
| C、NO |
| D、N2O3 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,11.2 L氯气所含原子数目为NA |
| B、2 L 0.2 mol/L的K2SO4溶液中K+数目为0.8NA |
| C、1 mol Fe作还原剂可提供电子数为2NA |
| D、标准状况下,NA个CO2分子和NA个H2O分子的体积相同 |