题目内容
17.在常温下,分别利用下列反应产生氢气,其反应方程式分别为:①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O
如果上述两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为( )
| A. | 8:5 | B. | 6:5 | C. | 2:1 | D. | 1:1 |
分析 ①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O,反应HCl中Cl元素从-1加升高到0价,10molHCl被氧化生成5molCl2;
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O反应HCl中Cl元素从-1加升高到0价,5molHCl被氧化生成3molCl2,据此分析.
解答 解:①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O,反应HCl中Cl元素从-1加升高到0价,10molHCl被氧化生成5molCl2,所以生成3molCl2需要6molHCl;
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O反应HCl中Cl元素从-1加升高到0价,5molHCl被氧化生成3molCl2,
则两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为6:5;
故选B.
点评 本题考查了氧化还原反应的计算,题目难度中等,注意根据反应中元素的化合价的变化分析,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
7.下列关于现象的说法正确的是( )
| A. | 向某溶液中加入氯水再滴加KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+ | |
| B. | 取某溶液进行焰色反应,透过蓝色钻玻璃焰色为紫色,则原溶液的溶质一定是KNO3 | |
| C. | 向某溶液中加入BaCl2溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液不一定含有SO42- | |
| D. | 往Na2CO3和NaHCO3溶液中滴加酚酞都变红,说明Na2CO3和NaHCO3都是碱 |
8.常温下,下列有关溶液中微粒浓度的判断正确的是( )
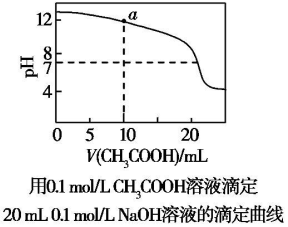

| A. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(CH3COONa)<c(Na2CO3)<c(NaOH) | |
| B. | H2A为弱酸,则0.1 mol.L-1NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| C. | 图中pH=7时:c(Na+)>c(CH3COO-)>c(OH-)=c(H+) | |
| D. | 上图中a点溶液:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) |
12.下列解释实验事实的方程式中,不准确的是( )
| A. | 在CH3COONa 溶液中滴入无色酚酞,溶液变红:CH3COO-+H2O?CH3COOH+OH- | |
| B. | 在Mg(OH)2白色悬浊液中滴入饱和FeCl3溶液,悬浊液变红褐:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| C. | 在NaHSO3溶液中滴加紫色石蕊溶液,溶液变红:NaHSO3=Na++H++SO32- | |
| D. | 在草酸溶液中滴入几滴稀H2SO4酸化的KMnO4溶液,溶液无色:2MnO4-+5H2C2O4+6H +=2Mn2++10CO2↑+8H2O |
2.下列离子方程式正确的是( )
| A. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag | |
| B. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| C. | 硫酸氢钠与氢氧化钠溶液混合:OH-+H+=H2O | |
| D. | 向澄清石灰水中加入盐酸:2H++Ca(OH)2=Ca2++2H2O |
9.下列有关胶体的说法正确的是( )
| A. | 直径介于10-9m~10-7m之间的微粒称为胶体 | |
| B. | 明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒 | |
| C. | 用聚光手电筒照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 | |
| D. | 将Fe(OH)3胶体和泥水分别进行过滤,发现均不能通过滤纸 |
6.反应A(g)+2B(g)?C(g)+D(g)+QKJ的能量变化如图所示,有关叙述正确的是( )
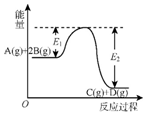

| A. | Q=E2 | |
| B. | 在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 | |
| C. | Q>0,升高温度,正反应速率增大,逆反应速率减小 | |
| D. | 若减小体积,平衡会移动,当反应再次达到平衡时,A的平衡浓度增大 |
19.室温下pH值相同的下列溶液中,浓度最大的是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | NaOH | D. | CH3COONa |
